当一位长期自认为A型血的个体突然被诊断为“熊猫血”(Rh阴性血型)时,这种看似矛盾的现象实则揭示了人类血型系统的复杂性与动态性。血型不仅是基因遗传的静态标签,更可能因基因突变、疾病干扰或检测技术局限而呈现出“变异”特征。这种特殊案例既挑战了传统认知,也推动着医学对生命密码的深度探索。

ABO与Rh系统的独立遗传
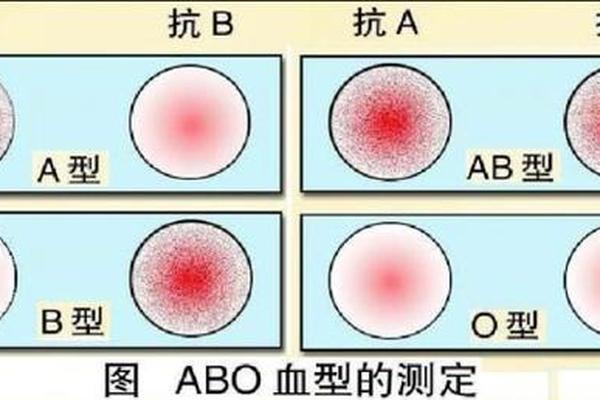
ABO血型系统与Rh血型系统是决定人类血液“身份”的两大核心体系。ABO系统由第9号染色体上的基因控制,通过红细胞表面A/B抗原的表达划分类型;而Rh系统则位于第1号染色体,其D抗原的存在与否定义了Rh阳性(+)或阴性(-)。若个体同时表现为A型(ABO系统)和Rh阴性(Rh系统),本质上属于两个独立系统的叠加结果,而非传统意义上的“变异”。
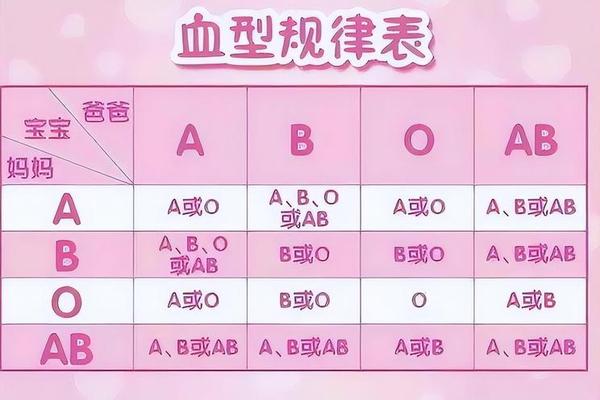
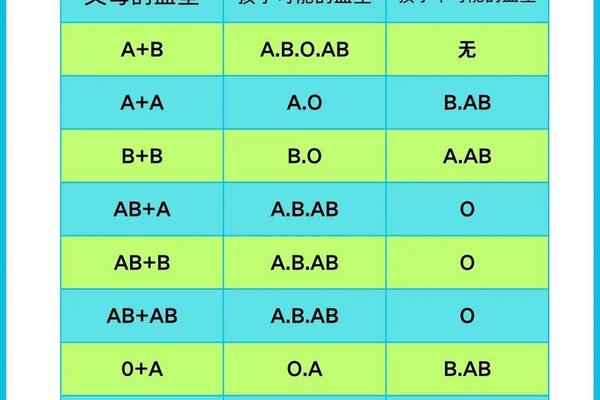
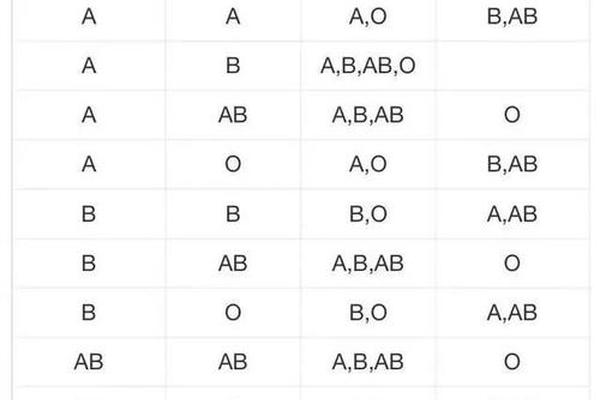
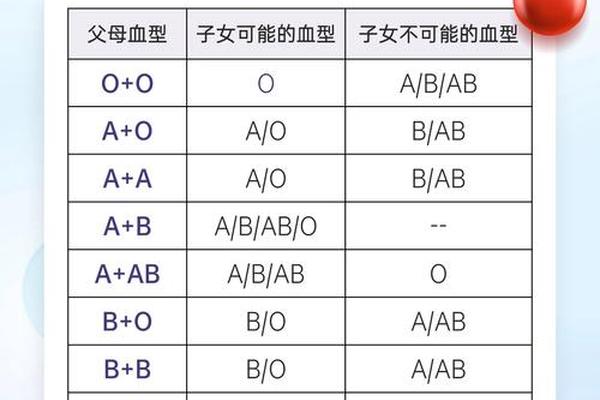
遗传学规律显示,Rh阴性由隐性基因dd决定。当父母均为携带Dd杂合基因的Rh阳性者时,子代有25%概率遗传dd组合,成为Rh阴性。例如,父母若为A型Rh阳性(Dd),孩子可能继承A型与dd组合,形成“A型熊猫血”的特殊状态。这种跨系统的基因组合,解释了为何ABO血型与Rh血型可以独立变化。
基因突变与抗原表达异常
真正的血型“变异”可能源于基因突变或抗原表达的动态改变。例如,D抗原的弱表达(Weak D型)或部分缺失(Partial D型)可能导致常规检测中将Rh阳性误判为阴性。2024年大连发现的B(A)亚型案例显示,基因c.797C>T突变使红细胞同时表达B抗原与弱A抗原,打破了兰德斯特定律的常规认知。
疾病因素也可能干扰血型判定。白血病患者因造血干细胞异常,可能暂时出现A/B抗原减弱,导致ABO血型检测偏差。但此类变化多为一过性,随病情缓解恢复原血型。值得注意的是,Rh系统的抗原变异更常由遗传而非后天因素驱动,真正的Rh阴性“后天获得”极为罕见。
检测技术局限与认知突破
血型误判常与检测方法局限性相关。常规血清学检测可能遗漏弱D型或Del型等特殊亚型。例如,Del型红细胞D抗原浓度仅为正常值的1/500,需通过吸收放散试验才能识别。2022年浙江大学儿童医院案例中,新生儿因母婴血型抗体干扰出现RhD“假阴性”,经多重检测技术复核才确认真实血型。
基因测序技术的进步为精准分型提供新路径。第三代单分子测序可识别传统方法无法检测的基因突变,如大连B(A)亚型的c.797C>T变异。这类技术突破不仅修正了既往认知,更揭示了人类已发现43种红细胞血型系统中仍存在大量未解之谜。
临床应对与未来展望
对于“A型熊猫血”群体,输血安全需遵循双重原则:ABO同型且RhD阴性。紧急情况下,男性或无生育需求女性可输注Rh阳性血,但会引发抗体产生,限制未来输血选择。孕妇若为Rh阴性,需在妊娠28周及分娩后注射抗D免疫球蛋白,预防胎儿溶血。
建立区域性稀有血型库至关重要。我国已通过志愿者网络形成“熊猫血”互助体系,采用自体血预存、冷冻红细胞库等技术应对突发需求。2024年,《自然·微生物学》报道的酶转化技术,通过嗜黏蛋白阿克曼菌酶组去除A/B抗原,或将实现通用型O型血的规模化生产,这为突破血型限制带来革命性希望。
生命密码的再认知
从A型到“熊猫血”的演变,本质是基因与环境交互作用的微观呈现。这种特殊现象既警示我们血型系统的动态复杂性,也凸显精准医疗时代多维度检测的必要性。未来,随着基因编辑、酶工程等技术的发展,人类或将重构血液资源的分配逻辑——从被动适配转向主动改造,让每一个生命都能突破“血型枷锁”,获得平等的生存权利。