人类对血液奥秘的探索始于1900年,当奥地利科学家卡尔·兰德施泰纳首次发现红细胞表面特异性抗原的存在,由此建立的ABO血型系统为现代输血医学奠定了基础。在这个分类体系中,A型血因其独特的抗原特性成为关键研究对象——其红细胞表面携带的A抗原既是免疫识别的重要标记,也是决定输血相容性的核心要素。当A抗原与相应抗体相遇时引发的凝集反应,不仅揭示了生命系统的精密调控机制,更成为临床安全输血必须跨越的生物学门槛。
一、A抗原的生物学基础
A型血的定义源于红细胞膜表面特异性糖蛋白结构的差异。在ABO血型系统中,A抗原的化学本质是糖脂分子末端的N-乙酰半乳糖胺,这种糖基通过α-1,3糖苷键连接在前体H抗原的寡糖链上。基因测序研究显示,A抗原的表达受控于9号染色体上的ABO基因位点,显性等位基因IA通过编码N-乙酰半乳糖胺转移酶,催化H抗原向A抗原的转化。
从分子进化角度看,A抗原的出现与人类免疫系统的适应性演化密切相关。比较基因组学研究表明,ABO基因在灵长类动物中具有高度保守性,提示这种抗原系统可能在病原体防御中发挥重要作用。血清学研究证实,A型个体血清中含有的抗B抗体,与B型红细胞表面的半乳糖基团发生特异性结合,这种互补式的免疫应答机制构成了ABO血型系统的分子基础。
二、A抗原的凝集机制
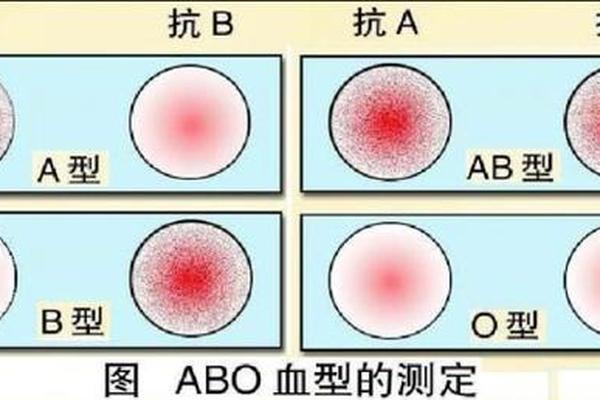
当A型红细胞遭遇抗A抗体时,糖蛋白抗原与免疫球蛋白的Fab段发生空间构象匹配,通过氢键和疏水作用形成抗原-抗体复合物。这种特异性结合会触发红细胞的交联反应,在显微镜下可见典型的凝集块形成。临床观察显示,1ml血浆中的抗A抗体足以引发10^8个红细胞的凝集,这种级联放大效应在输血反应中可能导致毛细血管阻塞和溶血性休克。
在ABO血型交叉配型试验中,A型受血者接受B型供血时,供体血浆中的抗A抗体与受体红细胞发生凝集反应的风险系数高达92%。值得注意的是,O型血作为"万能供体"的特殊地位源于其红细胞表面缺乏A、B抗原,但O型血浆中同时存在的抗A和抗B抗体仍可能引发受血者的迟发性溶血反应,这解释了现代临床医学严格推行同型输血原则的生物学依据。
三、血型遗传的分子密码
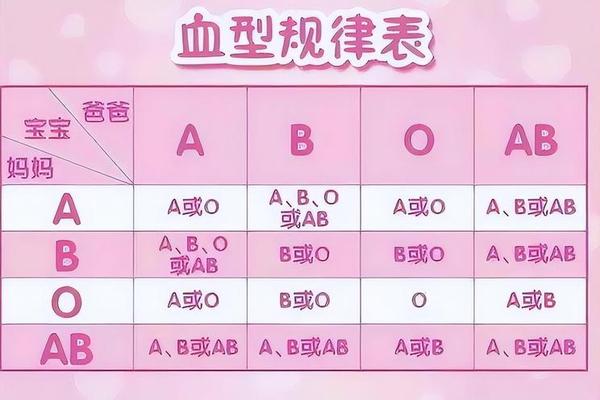
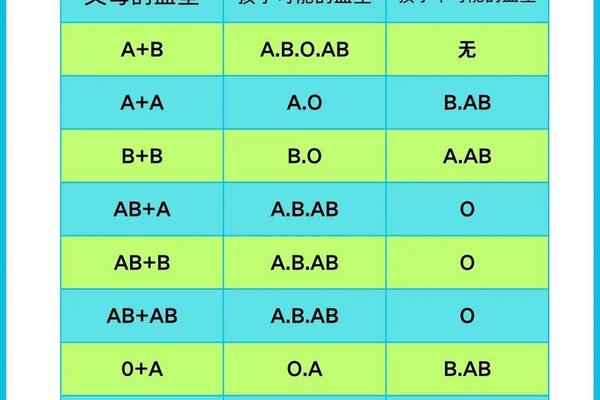
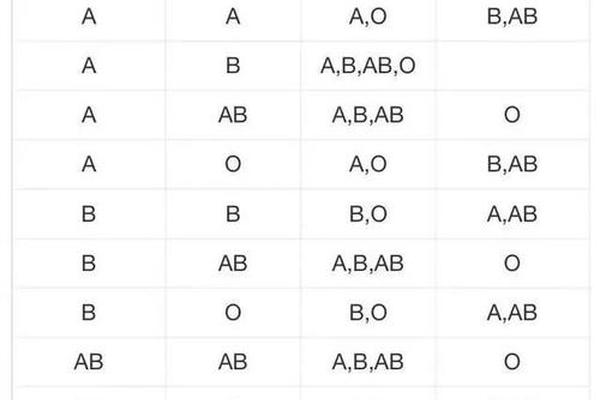
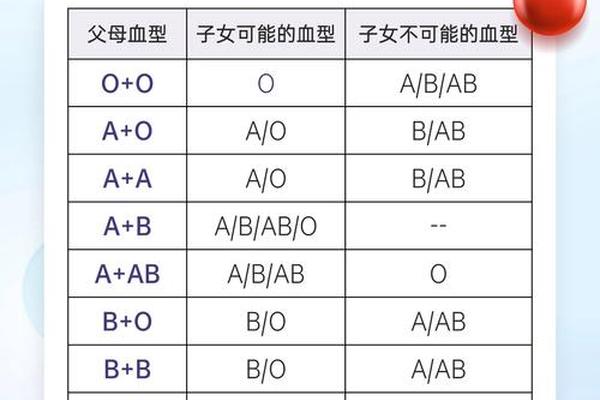
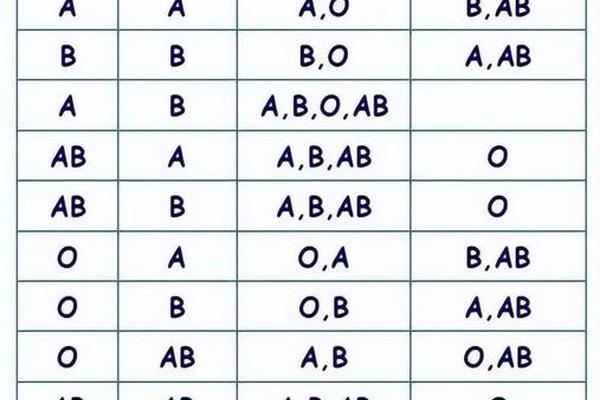
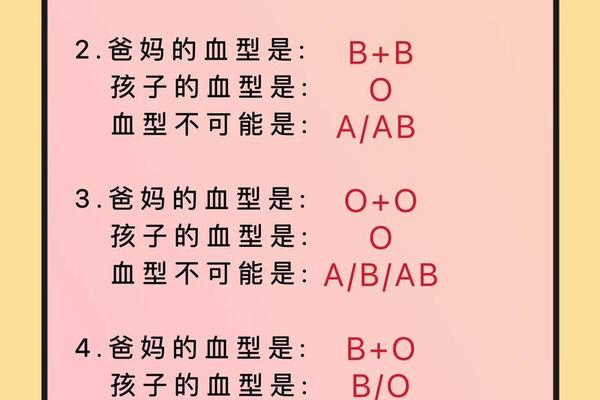
孟德尔遗传规律在ABO血型系统中得到完美诠释。IA基因作为显性等位基因,与隐性i基因组合时可稳定表达A抗原。当父母分别为AO和BO基因型时,子代出现AB型的概率达到25%,这种特殊的显性共表达现象揭示了血型系统复杂的遗传调控网络。全基因组关联研究(GWAS)发现,ABO基因座上的单核苷酸多态性(SNP)与凝血因子VIII水平存在显著相关性,这为解释A型血人群心血管疾病易感性提供了分子线索。
表观遗传学研究揭示了环境因素对血型表达的潜在影响。2023年《血液学杂志》报道的临床案例显示,造血干细胞移植后受体血型可完全转变为供体型,证实了造血微环境对红细胞抗原表达的调控作用。这种生物学现象为器官移植免疫耐受研究提供了新的视角,同时也提示临床输血需动态监测患者血型变化。
四、临床实践中的核心价值
在急诊医学领域,快速血型鉴定技术将A抗原检测时间缩短至3分钟。免疫层析试纸条通过胶体金标记的抗A单克隆抗体,可在床旁实现98.7%的检测准确率,这种技术进步显著提升了创伤急救的成功率。统计数据显示,严格执行交叉配血制度使输血相关性急性肺损伤(TRALI)发生率从1970年代的0.5%降至当前的0.08%。
器官移植领域的最新指南强调ABO血型相容性的动态评估。采用血浆置换术清除受体内抗A抗体的方案,使跨血型肝移植成功率提升至79%。值得注意的是,A型供体的肾脏在AB型受体内存活率显著高于其他组合,这种特殊免疫耐受现象正在推动移植免疫理论的革新。
五、前沿研究与未来展望
合成生物学正在重塑血型抗原的研究范式。2024年《自然·生物技术》报道的基因编辑项目,成功将猪红细胞表面的α-半乳糖抗原改造为人类A抗原,这项突破使异种输血可行性研究取得实质性进展。单细胞测序技术则揭示了A抗原表达的肿瘤特异性,在胃癌组织中检测到异常糖基化A抗原,这为开发靶向免疫疗法提供了新方向。
群体遗传学研究发现了A型血分布的地域特征。欧洲人群A型血占比达40%,而亚洲地区则呈现从西向东递减的趋势,这种差异可能与历史上瘟疫选择压力相关。正在进行的跨国队列研究试图建立血型-微生物组-疾病的三维关联模型,初步数据显示A型个体肠道菌群中双歧杆菌丰度与抗肿瘤免疫应答存在正相关。
从兰德施泰纳的原始发现到现代分子医学的深度解析,A抗原研究始终推动着血液医学的革命性进步。在精准医疗时代,血型系统与个体化用药、疾病预防的关联研究将持续深化。建议未来研究重点关注三个方面:建立多组学整合的血型功能图谱,开发通用型人工红细胞替代产品,探索血型抗原在神经退行性疾病中的病理机制。这些研究方向不仅关乎输血安全的终极目标,更将揭示生命密码中隐藏的健康奥秘。