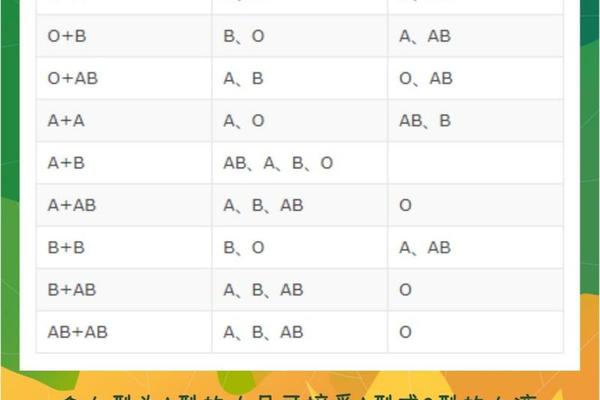
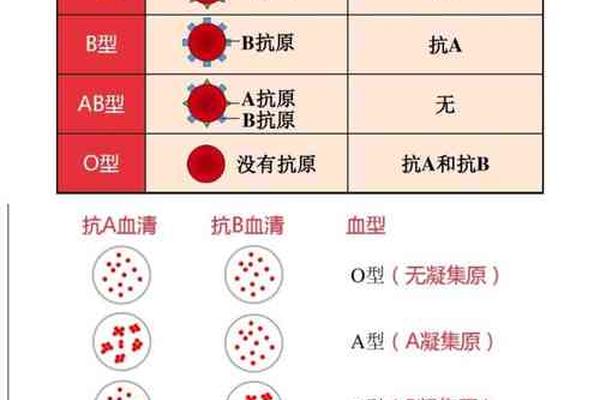
在ABO血型系统中,A型血个体的红细胞表面携带A抗原,而血清中则天然存在抗B抗体。这一现象源于人体免疫系统的自我识别机制:为避免红细胞凝集反应,血液中不会产生针对自身抗原的抗体。抗B抗体属于IgM型免疫球蛋白,分子量较大,由五个单体通过二硫键连接形成星形结构,这种结构使其具有更强的凝集能力,但无法通过胎盘屏障。
从分子生物学角度看,抗B抗体的形成与肠道菌群密切相关。研究表明,环境中某些细菌(如大肠杆菌)表面存在与B抗原相似的糖链结构,这些物质持续刺激人体免疫系统,促使B细胞分化为浆细胞并分泌抗B抗体。这种天然抗体的产生无需外源性抗原直接刺激,与后天获得的免疫性抗体(如Rh系统抗体)存在本质区别。值得注意的是,抗B抗体的效价会随着年龄增长而波动,婴幼儿时期效价较低,成年后逐渐升高至稳定水平。
抗B抗体的生理作用机制
抗B抗体在维持血液系统稳态中扮演双重角色。它通过识别异源性B抗原触发免疫防御。当B型红细胞进入A型个体血液循环时,抗B抗体的Fab段与B抗原特异性结合,通过激活补体系统导致红细胞溶解,或通过Fc段介导巨噬细胞的吞噬作用。这一机制有效防止异型输血引发的溶血反应,但也成为器官移植中血型匹配的重要考量因素。
抗B抗体还参与天然免疫屏障的构建。实验数据显示,A型血个体对某些携带B类抗原的病原体(如肺炎链球菌)具有更强的抵抗力,这可能与抗B抗体的交叉反应性有关。这种保护作用具有局限性,例如在ABO血型不合的移植中,供体淋巴细胞分泌的抗B抗体会攻击受体组织,引发移植物抗宿主病(GVHD)。
临床医学中的关键应用
在输血医学领域,抗B抗体检测是保障输血安全的核心环节。交叉配血试验通过将供血者红细胞与受血者血清混合,观察是否发生凝集反应,从而规避溶血风险。值得注意的是,A型血个体若接受AB型血液,虽然供血红细胞携带A、B双抗原,但供血血清中的抗A抗体会被受血者血浆稀释,因此少量输血仍被允许,这一原则被称为“次侧相容”。
在孕产医学中,抗B抗体效价监测对预防新生儿溶血症具有重要意义。尽管A型母亲的抗B抗体属于IgM型(通常不通过胎盘),但若母体因输血或流产史产生IgG型免疫性抗B抗体,则可能引发胎儿红细胞破坏。临床建议O型或A型孕妇在孕期定期进行抗体筛查,必要时通过血浆置换或免疫球蛋白注射干预。
抗体效价的动态变化与调控
抗B抗体水平受遗传与环境双重因素影响。基因层面,FUT1和ABO基因的多态性决定了个体抗原表达强度及抗体效价基线。例如,A2亚型个体的A抗原表达较弱,可能导致抗B抗体效价异常升高。环境因素中,肠道菌群组成、疫苗接种史以及既往输血经历均会通过表观遗传修饰影响抗体产生。
近年来,分子生物学技术的发展为抗体调控提供新思路。通过单细胞测序技术,研究者已鉴定出分泌抗B抗体的特定B细胞克隆,并探索CRISPR基因编辑技术在该领域的应用潜力。人工合成的B抗原类似物被用于诱导免疫耐受,在动物实验中成功降低抗B抗体效价,为器官移植开辟新途径。
总结而言,A型血清中的抗B抗体是人体精密免疫调控的产物,其生物学特性深刻影响着临床输血、器官移植和疾病防治。未来研究需进一步揭示抗体生成的分子开关机制,并开发精准调控技术。随着单细胞组学和基因编辑技术的进步,个性化血型医学将成为可能,例如通过体外修饰供体红细胞抗原或调控受体抗体效价,突破现有输血医学的局限性。这一领域的发展不仅需要基础研究的突破,更需建立多学科协作的转化医学平台,最终实现从理论创新到临床应用的跨越。