在医学实践中,输血是挽救生命的重要措施,而血型匹配则是保障输血安全的核心原则。A型血患者是否应当输入A型血,这一问题看似简单,实则涉及复杂的免疫学机制、临床操作规范以及特殊病例的挑战。随着输血医学的发展,人们对血型系统的理解不断深化,从单纯的ABO分型到Rh因子、抗体筛查等复杂检测,输血安全的标准也在逐步提高。本文将从多个维度探讨A型血输注的科学依据、潜在风险及临床应用,以期为临床实践提供参考。
一、ABO血型系统的基本原理
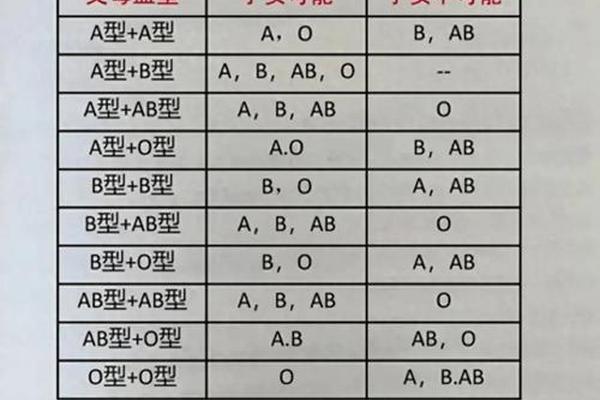
ABO血型系统是人类最早发现且最重要的血型分类方式。根据红细胞表面抗原的不同,ABO血型分为A、B、AB和O四型。A型血个体的红细胞表面携带A抗原,血浆中则含有抗B抗体。当A型患者接受A型血液时,供者红细胞上的A抗原与受者血浆中的抗B抗体不会发生反应,从而避免溶血风险。这种抗原-抗体的特异性匹配是ABO同型输血的免疫学基础。
ABO系统的复杂性不仅限于此。例如,A型血还可细分为A1和A2亚型,部分罕见亚型可能导致交叉配血困难。输血前必须通过正反定型实验确认血型,避免因抗原弱表达或抗体异常引发的误判。这些细节凸显了ABO系统在输血安全中的双重性:既是最基础的匹配原则,又需结合精准检测技术保障其可靠性。

二、Rh血型系统的潜在影响
Rh血型系统是仅次于ABO的第二大血型系统,其中D抗原的阳性或阴性状态对输血至关重要。若A型血患者为RhD阴性(俗称“熊猫血”),则必须输注RhD阴性的A型血,否则可能引发严重的溶血反应。临床案例显示,即使ABO血型相同,Rh系统的不匹配仍会导致致命后果。例如,一名A型血患者因体内存在抗E和类抗C抗体,无法接受普通A型血,最终依赖稀有血型库才找到相容血液。

多次输血可能刺激机体产生不规则抗体。研究发现,约30%的长期输血患者会因Rh系统其他抗原(如C、c、E、e)的差异发生免疫反应。Rh系统的全面检测已成为现代输血相容性试验的重要组成部分,仅依赖ABO同型已不足以保障安全。
三、临床操作规范与检测流程
根据《临床输血技术规范》,A型血患者输注A型血液需遵循严格流程。需采集患者输血前3天内的血样进行ABO和RhD复检,排除近期血型变异或抗体产生的可能。通过抗体筛查实验检测血浆中是否存在抗A1、抗D等不规则抗体。例如,部分A2亚型个体可能天然存在抗A1抗体,若输入A1型血将引发急性溶血。
交叉配血试验是最后一道安全屏障。即使供受双方ABO和RhD均匹配,仍需通过主侧(供者红细胞与受者血清)和次侧(受者红细胞与供者血清)试验验证相容性。统计显示,约0.1%的ABO同型输血因其他血型系统抗体导致配血不合,需启动疑难配血程序。这一流程的严谨性在武汉协和医院的案例中得到充分体现:患者虽为A型,但因罕见抗体需特殊筛选,最终通过稀有血型库锁定相容血液。
四、特殊情境下的挑战与对策
在紧急情况下,A型血供应不足可能迫使临床采取替代方案。研究指出,O型红细胞(需去除血浆)可作为A型患者的临时替代,但必须限量输注(成人不超过2单位)并密切监测溶血指标。这种操作存在争议:O型血浆中的抗A抗体可能引发迟发性溶血反应,尤其对免疫功能低下者风险更高。
对于需要多次输血的血液病患者,建议建立个性化输血档案。例如,白血病患者可能因化疗导致ABO抗原弱化,需采用增强技术(如LISS法)提高检测灵敏度。自体血回输、血液成分精准输注等新技术正在逐步普及,可减少异体输血带来的免疫风险。
五、未来研究方向与建议
随着基因组学的发展,血型鉴定正从血清学向分子检测迈进。全基因组测序可揭示Kidd、Duffy等300余种血型系统的详细信息,为精准配血提供新途径。人造血液研究取得突破,2023年英国团队成功将干细胞分化为功能性红细胞,未来或可解决稀有血型短缺问题。
临床实践中建议:1)加强输血前风险评估,对育龄女性、多次输血者优先进行扩展血型检测;2)建立区域性稀有血型动态数据库,实现快速响应;3)推广患者血液管理(PBM)理念,通过铁剂、促红素等减少输血需求。唯有技术创新与规范管理并举,才能实现输血安全与疗效的最大化。
总结
A型血患者输注A型血液在理论层面符合免疫相容性原则,但实际应用中需综合考量ABO亚型、Rh系统、不规则抗体等多重因素。现代输血医学已超越简单的血型匹配,发展为涵盖分子检测、抗体筛查、个体化治疗的精准体系。未来,随着新技术应用和管理模式优化,输血安全将迈向更高层次,为患者提供更可靠的保障。