在人类的血液中,每一个红细胞都携带着独特的生物密码,其中ABO和RhD血型系统的组合构成了个体最基础的血型身份标识。当体检报告单上出现"A型RhD+"的标注时,这个看似简单的符号背后,实则蕴含着复杂的生物学机制和重要的临床意义。作为最常见的血型组合之一,A型RhD+不仅是输血医学的重要参数,更是维系生命健康的安全密码。理解这个血型的本质,有助于我们更好地认识自身生理特征,在医疗救治中把握关键信息。
血型系统的双重密码
ABO血型系统是人类最早发现的血型分类体系,其核心在于红细胞表面A、B抗原的分布差异。A型血个体的红细胞膜上只携带A抗原,血浆中含有抗B抗体,这种特殊的免疫配置使得A型血只能接受同型或O型血的输入。而RhD血型系统则以D抗原的存在与否为判断标准,当红细胞表面存在D抗原时即为RhD阳性,这种特征在东亚人群中占比超过99%,属于绝对主流血型。
两个系统的叠加形成了完整的血型描述体系。在临床检验中,A型RhD+的确定需要经过双重检测:先用抗A、抗B血清确定ABO血型,再通过抗D试剂检测RhD抗原。现代分子生物学技术如多重PCR方法的应用,使得血型鉴定精度达到基因水平,能准确识别D/d基因型及其变异体。这种精准检测对输血安全和妊娠管理具有决定性意义。
临床医学的关键参数
在输血医学领域,A型RhD+的供血者承担着重要角色。由于A型血在我国占比约28%,RhD阳性又是绝对主流,这使得A型RhD+成为血库的主力储备。但需特别注意,RhD阴性患者若输入阳性血液,可能引发严重溶血反应,这种免疫排斥源于D抗原刺激产生的IgG抗体,其破坏力远超ABO系统的IgM抗体。
对妊娠妇女而言,RhD血型的检测关乎两代人的健康。当RhD阴性母亲怀有RhD阳性胎儿时,胎儿的红细胞可能通过胎盘刺激母体产生抗D抗体,导致新生儿溶血病。虽然A型RhD+孕妇无需担心此类风险,但知晓自身血型有助于医生制定更周全的产检方案。统计显示,我国新生儿溶血病例中,ABO血型不合占比80%,而RhD血型不合虽少但后果更严重。
遗传规律的显性表达
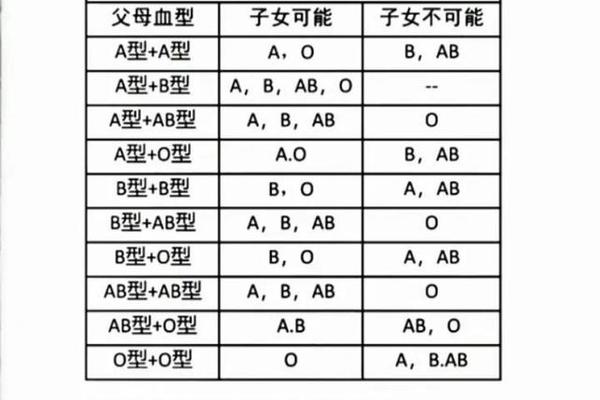
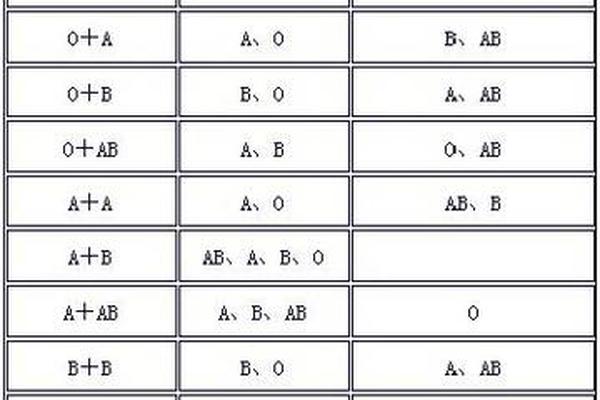
A型RhD+的遗传遵循孟德尔定律的双重组合。ABO系统中,A型可能由AA或AO基因型决定,当父母携带A基因时,子代有50%-100%概率遗传A型。RhD系统则呈现显性遗传特征,只要父母任一方携带D基因,子代即表现为RhD阳性。基因测序发现,汉族人群的RHD基因缺失率仅0.34%,这解释了RhD阴性的罕见性。
值得关注的是基因重组带来的特殊现象。约1%的RhD阳性个体实际携带RHD-CE-D等位基因,这类"亚洲型DEL表型"用常规血清学方法检测为阳性,但基因型实为杂合体。这类发现推动着血型检测技术从血清学向分子诊断演进,上海等地已建立多重PCR检测体系,能同时分析10个RHD基因外显子。
生物进化的生存印记
从人类学视角观察,A型血的演化与农业文明息息相关。考古基因研究表明,A等位基因在1.5万年前的新石器时代开始扩散,与人类从采集转向农耕的饮食结构变化同步。而RhD阳性则显示出明显的自然选择优势,在疟疾高发区,D抗原可能通过影响红细胞膜结构,增强对疟原虫的抵抗力,这种进化压力使得阳性基因在热带地区广泛保留。
跨种族比较揭示出血型分布的显著差异。我国藏族人群的RhD阴性率为4.7%,远高于汉族,这种差异与历史上的族群迁徙和隔离有关。而非洲某些部落的RhD阴性率可达5%,提示环境因素与遗传漂变共同塑造了血型多样性。
未来研究的突破方向
在精准医疗时代,血型研究正朝着分子机制深度探索。2019年《自然·遗传学》刊文揭示,ABO基因多态性与冠心病风险存在关联,A型血人群的血管内皮细胞更易发生脂质沉积。而RhD抗原的三维结构解析为人工血型改造提供可能,日本学者已成功利用干细胞技术培育出通用型红细胞。
针对我国人群特点的研究亟待加强。现有数据显示,0.1%的RhD阳性个体实际携带弱D变异型,这类人群输血时可能产生抗D抗体。建议建立全国性血型基因数据库,结合人工智能开发血型风险预测模型,这对稀有血型库建设和个性化输血具有重要意义。
理解A型RhD+血型的生物学本质和临床价值,不仅关乎个体健康管理,更是现代医学发展的微观缩影。从输血安全到疾病预防,从遗传咨询到进化研究,这个看似简单的血型标注背后,蕴藏着生命科学的深邃奥秘。随着单细胞测序和基因编辑技术的进步,人类终将揭开血型系统的全部密码,为医疗健康开辟新的可能。在此过程中,每个人对自身血型的认知和重视,都是构筑全民健康防线的重要基石。