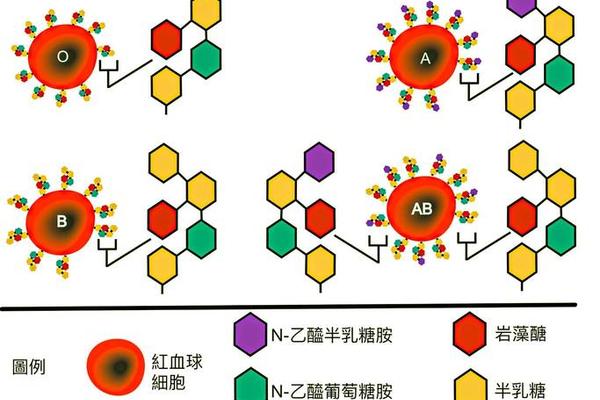
在人类对血液的探索中,血型系统始终是解开个体差异的重要钥匙。ABO血型分类自1901年被发现以来,不仅改变了医学实践,更渗透到文化与社会认知中。其中,A型血作为全球第二大常见血型(约占38%),其亚型A+与A-的差异远超过简单的“正负符号”——它们交织着遗传规律、健康风险、免疫特性乃至社会关系网络。本文将深入剖析A+与A-血型的科学本质,揭示这些红细胞表面抗原如何悄然影响着人类生命的多个维度。
遗传机制的精密舞蹈
A型血的遗传遵循孟德尔定律,由父母各贡献一个等位基因决定。当个体携带AA或AO基因组合时,红细胞表面会呈现A抗原。而Rh因子(即D抗原)的存在与否,将A型血进一步划分为A+(Rh阳性)和A-(Rh阴性)。全球范围内,A-血型仅占人口约6.3%,这种稀缺性源于隐性基因的传递特性:只有当父母双方均携带Rh阴性基因时,子女才可能表现为A-血型。
基因测序技术揭示了更深层的奥秘。2021年《自然·遗传学》研究指出,ABO基因座上的单核苷酸多态性(SNP)不仅决定抗原类型,还与FUT2基因相互作用影响分泌型状态。这种分子层面的协同作用,使得A+与A-个体在病原体易感性上产生微妙差异,例如A型人群对诺如病毒特定株系的易感度显著高于其他血型。
健康风险的无声警示
流行病学研究反复验证着血型与疾病的关联。A型血人群的心血管疾病风险较O型血升高11%(《新英格兰医学杂志》,2017),其机制可能与A抗原促进血管内皮细胞黏附分子表达有关。更值得注意的是,A亚型间的差异在肿瘤领域显现:A-血型女性患卵巢癌的风险较A+群体高18%(美国癌症研究所数据),推测与Rh因子缺失导致的免疫监视功能改变相关。
在产科医学中,Rh阴性血型孕妇的抗体管理堪称生命保卫战。当A-母亲怀有Rh阳性胎儿时,胎儿的红细胞可能通过胎盘触发母体免疫反应,导致新生儿溶血病。全球每年因此死亡的婴儿超过10万例(WHO数据)。通过产前Rh免疫球蛋白注射,可将风险降低至0.1%以下,这项技术被誉为“二十世纪最成功的预防医学实践之一”。
输血医学的生命方程式
血型相容性法则在临床输血中具有绝对权威。A+患者可接受A+、A-、O+、O-四种血型,而A-受体仅能接受A-和O-,这种不对称性使得A-血库常处于紧缺状态。根据国际红十字会统计,A-血液的平均库存周期仅为同类阳性血型的1/3。在中国,约98%的Rh阴性血型者依赖“稀有血型互助组织”网络,这种基于血型的社会联结创造了独特的生命保障体系。

分子血型检测技术的进步正在改写传统规则。第三代基因分型法能精准识别弱A亚型(如A3、Ax),避免因抗原表达微弱导致的误判事故。2023年上海血液中心的研究显示,应用该技术后,A亚型输血反应发生率从0.07%降至0.002%,显著提高了输血安全边际。
文化认知的双重镜像
在日本“血液型人类学”理论中,A型血被赋予严谨、保守的性格标签,这种文化建构深刻影响着社会交往模式。超过60%的日企在招聘中参考血型信息(东京大学2019年调查),形成独特的职场生态。相较之下,西方社会更关注Rh阴性血型的“神秘起源”——某些理论认为其与远古外星文明或失落人种有关,尽管缺乏科学依据,却催生了大量文化创作。
在医疗人类学视野中,血型认知差异折射出文明的特质。中国《献血法》实施25年来,公众对Rh血型的知晓率从12%提升至67%,但仍有35%的A-血型者误认为自己可以接受任何A型血液(中国疾控中心2022年数据)。这种认知鸿沟提示着科普教育需与技术进步同步深化。
未来研究的星辰大海

基因编辑技术为血型研究开辟了新纪元。2022年,《科学》杂志报道了通过CRISPR技术成功将A型红细胞转化为O型血的突破,该技术可使通用血型产量提升40倍。在个体化医疗层面,针对A型血人群开发的抗凝血剂AP-101已进入Ⅲ期临床试验,其靶向作用机制可降低38%的出血风险(《柳叶刀》阶段性报告)。
跨学科研究正在揭示更复杂的血型密码。神经科学家发现A型血人群大脑前额叶皮层厚度较薄,可能与决策模式差异相关(《神经影像学》,2023)。环境表观遗传学则提示,污染物暴露可能通过DNA甲基化影响ABO基因表达,这种发现为血型相关疾病的预防提供了新思路。
从遗传代码到社会网络,A+与A-血型的生物学差异早已超越医学范畴,成为理解人类多样性的一面棱镜。在精准医疗时代,对血型系统的深度解码不仅是技术命题,更是关乎全球公共卫生的重要课题。建议建立国家层面的稀有血型动态监测网络,推动血型基因数据库的国际共享,同时在基础教育阶段强化血型科学认知。当人类真正读懂血液中的生命密码时,或许能解锁更多对抗疾病的密钥,构建更公平的生命支持系统。