在人类对血型认知的百年历程中,ABO血型系统始终是医学研究的核心领域。当人们普遍认为血型终生不变时,一系列临床案例却揭示了血型系统的复杂性——某些情况下,A型血可能因基因突变或病理因素呈现异常状态,甚至被误判为其他血型。这种被称为"血型异常"的现象,不仅挑战了传统认知,更在输血医学、遗传学等领域引发深刻反思。从南京准妈妈携带全球首例A3亚型基因,到白血病患者血型抗原的神秘消失,这些特殊案例犹如打开潘多拉魔盒,暴露出人类对生命密码解读的局限。
血型异常的定义与分类

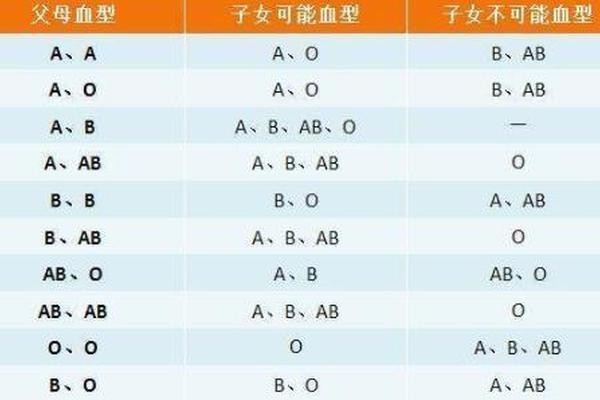
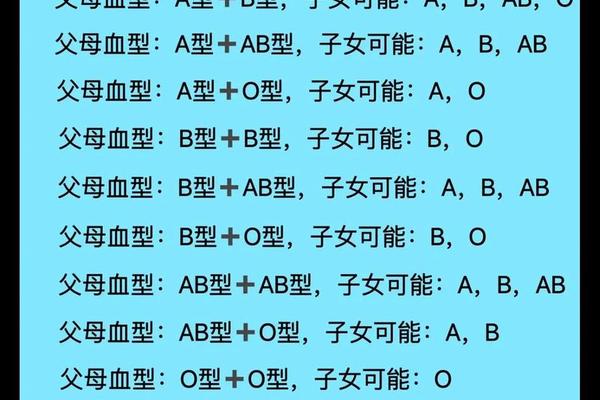
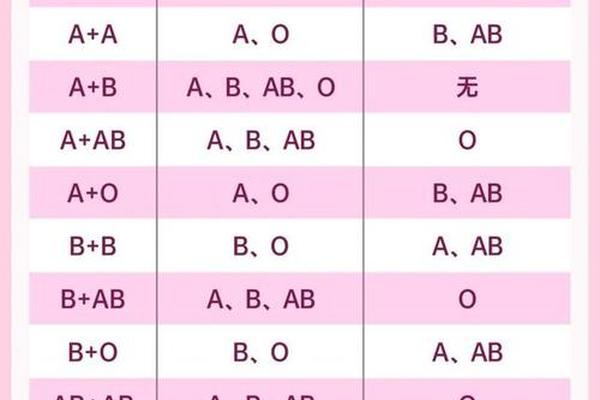
血型异常指在特定条件下,个体血型抗原表达或抗体产生出现偏离常规的现象。这种变异可分为病理性与遗传性两类:前者由疾病诱发,如恶性肿瘤细胞分泌类血型物质干扰检测;后者源于基因突变,如ABO基因座上的新型等位基因导致抗原结构改变。以A型异常为例,正常A型抗原由N-乙酰半乳糖胺构成,但在亚型中可能因转移酶活性降低,出现抗原表达减弱的A2、A3等变异型。
国际输血协会数据显示,ABO系统已发现380余种等位基因,这些基因的微小突变可能引发抗原结构的"蝴蝶效应"。例如南京发现的A3亚型,其基因序列中单个碱基突变导致编码酶活性降低,使红细胞表面A抗原密度仅为正常值的30%。这种分子层面的改变,在血清学检测中易被误判为弱A型或AB型,揭示出血型系统的精妙与脆弱并存。
A型异常的遗传学机制
ABO基因位于9号染色体q34区域,其突变可能改写血型命运。正常A型基因编码的α-1,3-N-乙酰半乳糖胺转移酶,负责将特定糖基连接到H抗原上。当基因发生移码突变或错义突变时,酶的三维结构可能发生畸变。江苏血液中心发现的A3亚型案例中,正是第7外显子的点突变导致酶活性位点改变,使得抗原合成效率大幅下降。
这类突变具有随机性与遗传性双重特征。韩国曾报道父母均为B型却诞下AB型婴儿的案例,基因测序显示子代ABO基因存在自发突变。统计表明,约0.01%的东亚人群中存在未被识别的ABO新等位基因。这些"基因幽灵"潜伏在人类基因组中,可能在世代传递中突然显现,打破常规遗传规律。如广东某家庭因父亲携带B亚型基因,导致亲子血型"不符",凸显基因检测在当代医学中的必要性。
疾病与血型异常的关联
病理状态可能引发暂时性血型异常。白血病患者中,约15%会出现ABO抗原减弱现象,其机制涉及恶性克隆细胞对造血微环境的破坏。这些患者的红细胞表面抗原密度可能降至检测阈值以下,在输血配型时造成假阴性结果。更特殊的是多发性瘤患者,其血浆中异常免疫球蛋白可能中和标准抗血清,导致血型鉴定出现"魔术般"变化。
母婴血型不合构成另一种风险情境。当A型孕妇携带抗B抗体时,若胎儿遗传父亲B型基因,可能引发新生儿溶血。江苏省血液中心的研究显示,约0.3%的妊娠存在潜在血型不合风险。而血型亚型的误判可能放大这种风险,如将A3亚型误判为O型时,母体抗A抗体可能攻击胎儿红细胞。这种隐蔽的威胁,要求产科建立更精准的血型筛查体系。
血型检测的技术革新
传统血清学检测正面临分子诊断技术的挑战。南京案例中,常规检测无法确定准妈妈血型,最终通过基因测序发现新型突变。二代测序技术可识别ABO基因中0.1%的稀有变异,将检测灵敏度提升百倍。日本建立的ABO单倍型数据库,已收录超过200种基因变异模式,为精准输血提供分子图谱。
质谱技术的引入开创了新维度。通过分析红细胞膜糖蛋白的糖链结构,研究者能区分A1与A2亚型的细微差异。美国血库协会建议,对造血干细胞移植患者应采用"血清学+基因型"双重验证。这些技术进步不仅破解了诸多血型谜案,更推动输血医学进入个体化时代。
临床意义与未来展望
血型异常对临床实践构成双重挑战。误判血型可能引发致命性输血反应,研究显示0.02%的输血事故源于罕见血型未被识别。而精准识别血型变异具有抢救价值:某淋巴瘤患者因检出B亚型,成功获得匹配的稀有血液。建立区域性稀有血型库、开发快速基因分型试剂盒,已成为输血安全的新防线。
未来研究应聚焦于血型变异的分子调控网络。表观遗传学研究发现,DNA甲基化可能影响ABO基因表达。基因编辑技术为血型改造带来曙光,日本学者已实现体外诱导iPS细胞表达特定血型抗原。随着单细胞测序技术的普及,人类或将绘制出完整的血型变异图谱,为每个个体定制"血液身份证"。
血型系统的复杂性印证了生命的深邃。从卡尔·兰德施泰纳发现ABO血型,到今日基因测序揭示的分子奥秘,人类在破解生命密码的征程中不断遭遇认知边界。那些看似异常的血型变异,实则是生命多样性的自然呈现。在精准医学时代,唯有以敬畏之心探索这些"异常",才能让输血医学真正实现"滴滴精准,生命相承"的承诺。