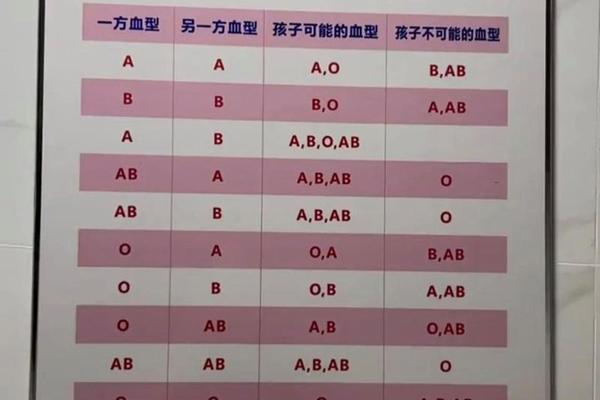
在人类复杂的血型系统中,ABO与Rh血型是最具临床意义的分类体系。当我们将这两个系统交叉观察时,会发现一个有趣的现象:ABO系统中的A型血人群,同样可能携带Rh阴性这种被称为“熊猫血”的稀有血型。这种血型组合的罕见性不仅源于遗传机制的特殊性,更与不同种族的基因分布密切相关,其背后隐藏着人类进化与医学实践的双重密码。

一、血型系统的独立性原理
ABO血型与Rh血型分属不同的遗传系统,这种独立性构成了二者组合的理论基础。从基因定位来看,ABO血型基因位于第9号染色体,而决定Rh血型的RHD基因则位于第1号染色体,两者在遗传过程中遵循孟德尔自由组合定律。这意味着父母在传递血型基因时,ABO系统的显隐关系与Rh系统的D/d基因分离互不干扰。
在分子机制层面,ABO系统的抗原形成依赖于糖基转移酶的作用,而Rh系统的D抗原本质是跨膜蛋白。这种生化性质的差异使得两个系统的抗原表达互不影响。临床检测数据显示,我国汉族人群中A型血占比约28%,而Rh阴性仅占0.3%-0.4%。根据概率乘积计算,A型Rh阴性的理论发生率约为0.084%,即每万人中不足1例,这种低概率正是系统独立性的直接体现。
二、隐性遗传的叠加效应
Rh阴性血型的形成需要双隐性基因型(dd),这种遗传特性与ABO系统中的显性遗传形成鲜明对比。当个体同时携带A型血的显性基因(IA)和Rh阴性的隐性基因(dd)时,就会表现出A型Rh阴性的特殊表型。家系研究表明,若父母中一方为Rh阳性杂合子(Dd),另一方为Rh阴性(dd),子女出现Rh阴性的概率可达50%。
这种遗传特性在跨种族通婚中表现尤为显著。例如白种人Rh阴性比例达15%,当高加索人种与东亚人种结合时,其后代既可能继承父系的A型血基因,也可能获得母系的Rh阴性基因。2017年我国某三甲医院报告的罕见血型案例中,就存在父母均为Rh阳性杂合子却生育出Rh阴性子女的情况,这充分证明了隐性基因的潜伏性。
三、地域与种族的分布差异
全球血型分布图谱显示,A型Rh阴性的出现频率存在显著地域差异。在Rh阴性比例较高的巴斯克地区(约35%),A型Rh阴性占比可达5.25%,而在我国,由于Rh阴性基因频率仅0.3%-0.4%,导致A型Rh阴性成为真正的“万分之遇”。这种差异与历史上的遗传漂变密切相关——冰河时期欧洲大陆的种群瓶颈效应,使得Rh阴性基因得以保留并扩散。
分子人类学研究揭示了更深层的进化密码。对古代人骨DNA的分析表明,新石器时代东亚人群的Rh阴性基因频率不足0.1%。而印欧语系人群向东亚的迁徙,带来了D基因突变的新类型。现今我国山西、河南等地相对较高的Rh阴性比例,正与古代欧亚游牧民族的活动轨迹相吻合。
四、临床医学的特殊意义
对于A型Rh阴性个体而言,血型稀有性带来的临床挑战尤为突出。输血医学数据显示,该类患者需要输血时,寻找到完全匹配的A型Rh阴性供体的成功率不足0.01%。更严峻的是妊娠风险——Rh阴性母亲若孕育Rh阳性胎儿,抗D抗体可通过胎盘引发新生儿溶血病,这种情况在二胎中的发生率比首胎高出20倍。
现代医学已发展出针对性解决方案。通过产前RHD基因分型技术,可在妊娠早期确定胎儿Rh状态。对于高风险孕妇,Rh免疫球蛋白(抗D球蛋白)的预防性注射可使新生儿溶血病发生率降低至0.3%以下。我国部分中心城市建立的“稀有血型互助网络”,通过冻存自体血、建立动态数据库等方式,有效改善了A型Rh阴性患者的医疗安全。
从遗传学的独立法则到临床医学的精准干预,A型Rh阴性血型的存在既印证了生物多样性的奇妙,也凸显了现代医疗体系应对特殊需求的能力。这种血型组合的稀有性不应被视为缺陷,而应作为推动血型研究、完善应急机制的特殊契机。未来随着基因编辑技术的发展,定向修饰Rh基因或将成为解决输血困境的新途径,但在此过程中,如何平衡技术与医疗公平,将是医学界需要深思的课题。