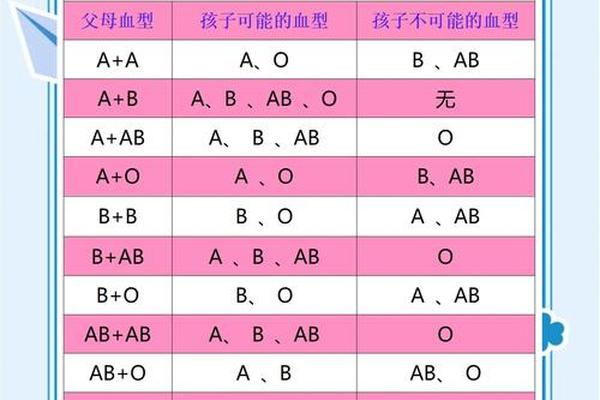
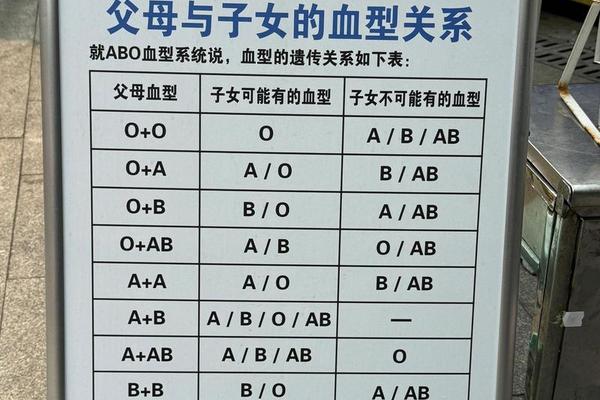
A型Rh阴性血型是人类血型系统中极为罕见的组合。根据统计,中国汉族人群中Rh阴性血型的比例仅为3-4‰,而A型血约占中国人口的31%。若将两者结合,A型Rh阴性个体的比例可能低至0.1‰左右,相当于每万人中仅有1人。这种稀有性源于Rh血型系统的复杂遗传机制:RhD基因的缺失或失活导致红细胞表面缺乏D抗原,而A型血则由ABO系统中的显性基因决定。两者的独立遗传规律使得A型Rh阴性成为“双重筛选”的结果。
值得注意的是,Rh阴性血型的分布存在显著种族差异。例如,白种人中Rh阴性比例约为15%,非洲裔人群为5-8%,而巴斯克人甚至高达40-50%。这种差异可能与早期人类迁徙中的遗传漂变有关。在冰河时期,欧洲旧石器时代人类几乎灭绝,仅巴斯克地区的幸存者保留了高频率的Rh阴性基因,并通过奠基者效应延续至今。相比之下,东亚人群的Rh阴性基因频率在历史进程中可能因自然选择压力而逐渐降低。
二、临床医学中的双重挑战
对于A型Rh阴性女性而言,妊娠可能引发新生儿溶血病(HDN)。当母体为Rh阴性而胎儿遗传了父亲的Rh阳性基因时,母体免疫系统会将胎儿红细胞视为异物,产生抗D抗体。首次妊娠时抗体效价较低,但二次妊娠时抗体可通过胎盘屏障攻击胎儿红细胞,导致贫血、核黄疸甚至胎死宫内。研究显示,1968年前欧洲Rh阴性产妇发生HDN的几率达5%,死亡率高达40%。随着抗D免疫球蛋白的普及应用,目前该风险已降至1%以下,但产前筛查和预防性用药仍是必要措施。
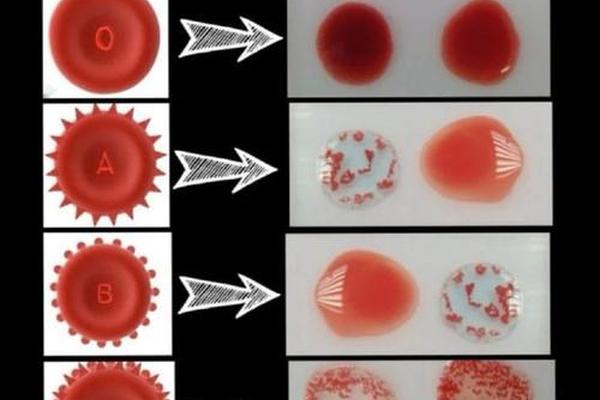
输血安全是另一重大挑战。A型Rh阴性患者若误输Rh阳性血液,可能引发急性溶血反应。这种特殊性要求医疗机构必须建立双重核查机制:既需匹配ABO系统,又要确保RhD抗原阴性。据统计,全球仅0.3%的献血者为A型Rh阴性,血液储备常处于临界状态。例如中国稀有血型联盟建议,接到用血需求时应优先核实信息、统筹调配,避免因集中捐献造成血液过期浪费。
三、社会支持系统的特殊需求
建立动态血液储备网络至关重要。由于全血保存期仅35天,成分血保存期更短,A型Rh阴性血的应急供应需要精准管理。部分国家采用“冰冻红细胞”技术延长保存至10年,但解冻洗涤过程会损失15%红细胞,且成本高昂。中国稀有血型联盟提出的“三级响应机制”具有借鉴意义:轻度需求由地方血站解决,中度需求启动区域调剂,重度需求则启动全国联网。
公众认知提升同样迫在眉睫。调查显示,约60%的Rh阴性血型者首次知晓自身血型是通过偶然体检,而非系统筛查。这种现象导致部分孕妇直至妊娠中期才发现血型不合风险。建议将Rh血型检测纳入婚前检查常规项目,并通过基因检测技术提前识别潜在风险。建立终身血型档案、开发智能提醒系统等措施,可帮助A型Rh阴性人群及时获得医疗支持。
四、进化谜题与未来研究方向

从进化生物学视角看,Rh阴性血型的存在本身是个悖论。新生儿溶血病造成的负向选择理论上应逐渐淘汰该基因,但其在全球范围内的持续存在提示可能存在未被发现的进化优势。捷克学者提出的“弓形虫假说”认为,Rh阳性个体对弓形虫感染引发的神经行为异常更具抵抗力,这种优势可能平衡了HDN的负面影响。但争议依然存在,因为D抗原并不直接参与神经信号传导,且相关研究多基于回顾性数据分析。
未来研究可聚焦于多组学技术的整合应用。通过全基因组关联分析(GWAS)寻找与Rh阴性相关的其他功能基因;利用单细胞测序技术解析RhD基因在胚胎发育中的表达模式;结合考古DNA数据追溯Rh阴性基因的迁徙路径。开发通用型人工血液或基因编辑技术修复RhD基因缺陷,可能从根本上解决输血难题。
A型Rh阴性血型既是生命馈赠的特殊印记,也是医学领域的独特课题。其稀有性既源于遗传规律的偶然组合,也折射出人类进化长河中的选择压力。当前,通过完善血源管理、强化产前干预、推进基础研究等多维度努力,我们正在搭建起连接稀有血型个体与现代医学的桥梁。未来,随着基因技术的突破和社会支持体系的成熟,这一特殊群体将获得更全面的健康保障,其背后的生物学奥秘也有望被逐步揭开。正如巴斯克人的基因密码诉说着万年前的生存史诗,A型Rh阴性血型的研究将继续书写人类对抗生命挑战的新篇章。