在医学领域中,血型与溶血反应的关系一直是备受关注的课题。ABO血型系统作为人类最早发现的血型分类系统,其抗原与抗体的相互作用直接决定了溶血发生的可能性。其中,A型血作为ABO系统中的重要类型,其溶血风险常引发讨论:当父母均为A型血时,胎儿是否存在溶血风险?A型血个体是否比其他血型更易发生溶血?这些问题不仅涉及遗传学机制,还与临床诊疗和母婴健康息息相关。本文将从多个维度剖析A型血溶血的核心问题,结合最新研究证据,为读者提供科学解读。
ABO溶血的机制与分类
ABO溶血的发生源于母婴血型不合引发的免疫反应。当母亲体内缺乏胎儿红细胞携带的抗原时,母体会产生特异性抗体(如IgG),这些抗体通过胎盘进入胎儿血液后,攻击胎儿红细胞导致溶血。根据网页1的阐述,我国新生儿溶血症中ABO溶血占比最高,且多见于母亲为O型、胎儿为A或B型的情况。值得注意的是,A型血个体的溶血风险需分情况讨论:若母亲为A型血,胎儿同为A型,则不会发生ABO溶血;但若母亲为O型或Rh阴性,胎儿为A型,则可能触发免疫反应。
从血型抗原的分子结构来看,A型抗原由N-乙酰半乳糖胺构成,其抗原性较B型更强(网页41)。这解释了为何母体O型(天然含抗A、抗B抗体)与胎儿A型组合的溶血发生率更高。Rh血型系统的影响也不容忽视,Rh阴性母亲若怀有Rh阳性胎儿,可能引发更严重的溶血反应,但这类情况在汉族人群中较为罕见。
A型血溶血的特定风险
尽管A型血本身并非溶血的直接诱因,但在特定组合下风险显著增加。网页16指出,若父母均为A型血,但携带隐性O型基因(如AO基因型),胎儿可能遗传O型血。此时若母亲为O型且存在抗A抗体,仍可能发生ABO溶血。这一现象打破了“同型父母无风险”的认知误区,强调了基因检测在孕前评估中的重要性。
临床数据显示,A型血新生儿溶血的严重程度存在个体差异。网页1提到,约25%的ABO溶血患儿在出生24小时内出现黄疸,5%发展为重度贫血。而网页64的队列研究显示,孕妇血清IgG抗A效价≥1:128时,新生儿溶血风险增加4.5倍。这提示抗体效价监测对预后评估具有关键作用。A型抗原的强免疫原性可能导致更快的抗体生成速度,使得部分病例在第一胎即发病。
遗传因素与溶血概率
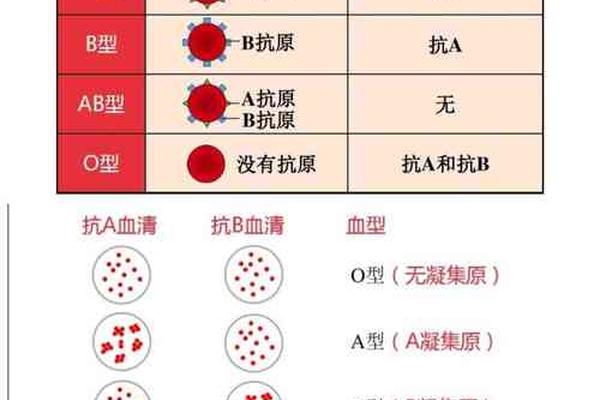
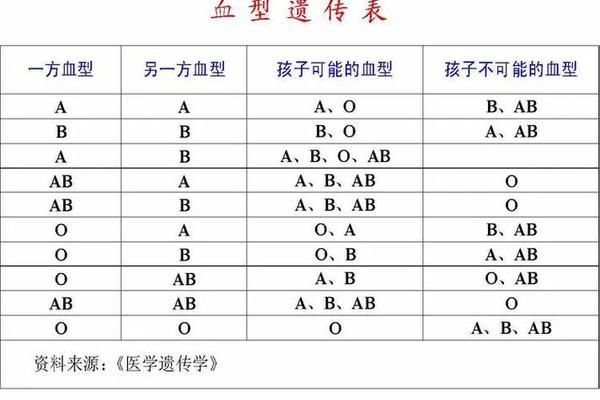
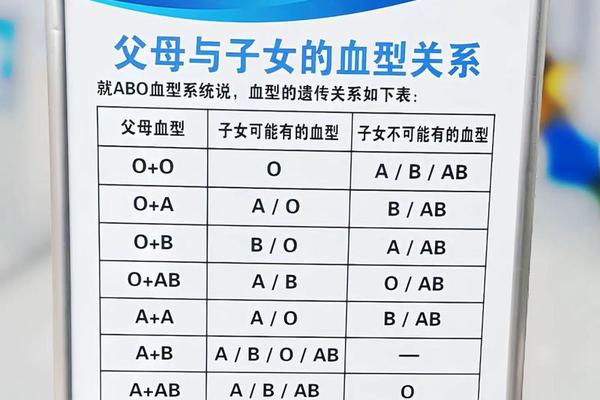
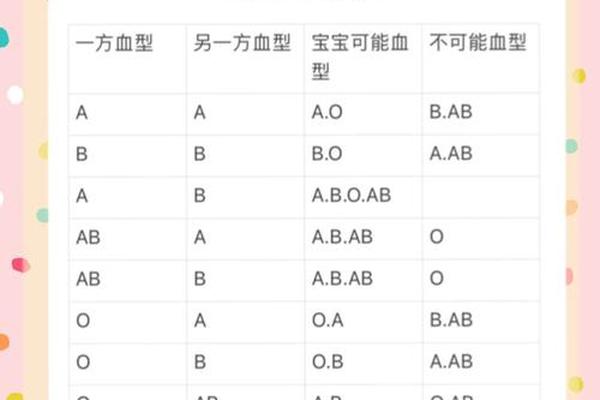
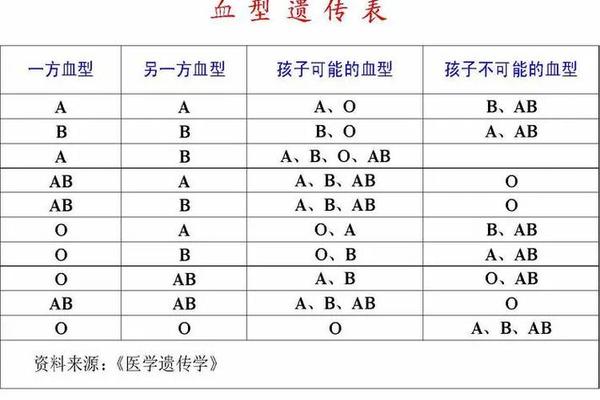
ABO血型的遗传遵循孟德尔定律,父母血型组合直接影响胎儿抗原表达。当父母均为A型(AA或AO基因型)时,胎儿可能为A型(75%)或O型(25%)。网页41详细阐释了A型等位基因(IA)通过编码α-1,3N-乙酰氨基半乳糖转移酶,催化H抗原转化为A抗原的生化过程。若胎儿遗传O型,则保留H抗原,此时若母亲为O型血,其体内天然存在的抗A抗体仍可能攻击胎儿红细胞。
值得注意的是,血型抗体的产生还与环境抗原暴露相关。网页1指出,自然界中存在的类A抗原物质(如某些细菌多糖)可能提前致敏O型血母亲,使其在初次妊娠时即产生IgG抗A抗体。这种“预致敏”现象解释了为何ABO溶血可发生于第一胎,而Rh溶血多出现于经产妇。基因与环境因素的交互作用,使得A型血溶血的预防需采取个性化策略。
临床管理与预防策略
对于A型血相关溶血风险,临床已建立系统的防控体系。孕前建议夫妻进行血型筛查,特别是O型或Rh阴性女性。网页27强调,孕期定期检测抗体效价(孕16周起每2-4周一次)可动态评估风险,当效价≥1:64时需加强监测。近年来,基于孕妇血浆游离DNA的胎儿血型基因分型技术(网页19)显著提高了产前诊断的准确性,减少侵入性操作的风险。
治疗方面,光照疗法仍是ABO溶血的首选干预手段,可有效降低胆红素水平(网页1)。对于重症病例,换血治疗能快速清除致敏红细胞和抗体。网页64的研究证实,联合网织红细胞计数与胆红素动态监测,可提升早期诊断率。中药制剂(如茵陈蒿汤)在降低抗体效价方面显示出辅助治疗价值。
综合现有证据,A型血个体是否易发溶血取决于特定的血型组合与环境暴露,而非单纯由A型抗原决定。父母同型(AA)的胎儿溶血风险极低,但携带隐性O基因的A型夫妇需警惕隔代遗传带来的血型不合。未来研究可聚焦于以下方向:一是开发更灵敏的抗体效价检测技术,实现风险精准分层;二是探索基因编辑技术在Rh阴性孕妇中的应用潜力;三是建立区域性血型数据库,优化溶血病的流行病学防控网络。
从临床实践角度,建议育龄夫妇将血型检测纳入常规孕前检查,高危孕妇建立专项健康档案。公众教育方面,需纠正“同型父母绝对安全”的认知偏差,提高对隐性基因遗传规律的理解。唯有通过医学研究的持续突破与公共卫生体系的协同优化,才能为新生儿构筑更坚实的健康屏障。