在医学领域中,血型不仅是人体独特的生物学标识,更与健康管理、临床救治等密切相关。除了广为人知的ABO血型系统外,Rh血型系统的阴性与阳性之分,造就了“稀有血型”这一特殊群体。其中,A型Rh阴性血型和被称为“熊猫血”的Rh阴性O型血,因稀缺性备受关注。本文将从多个角度解析这两种血型的科学定义、分布特点及社会意义,揭开其背后的医学奥秘。
定义与分类:血型系统的双重密码
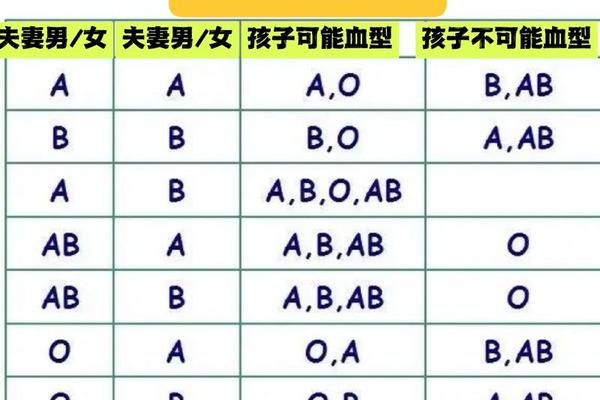
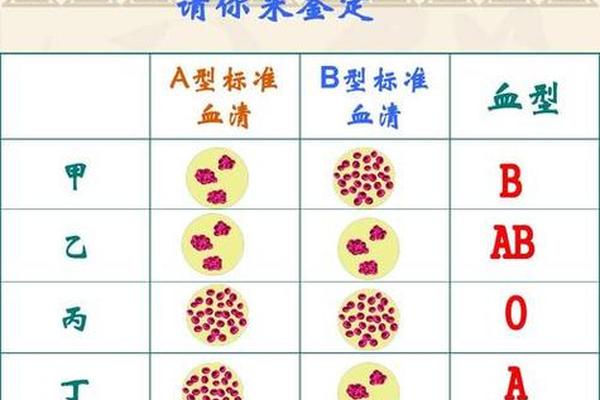
血型系统由ABO和Rh两大核心构成。ABO系统将人类血液分为A、B、AB、O四类,而Rh系统则通过红细胞表面是否存在D抗原来区分阴阳性。A型Rh阴性血型即同时满足ABO系统中的A型特征和Rh系统中的D抗原缺失,而Rh阴性O型血则是O型与Rh阴性特征的叠加,因其罕见性被称为“熊猫血”。
Rh阴性血型的命名源于恒河猴(Rhesus macaque)实验中的发现,其本质是红细胞缺乏D抗原。根据中国汉族人群的数据,Rh阴性比例仅为0.3%-0.4%,而O型Rh阴性在其中的占比更是不足万分之一,稀有程度堪比国宝熊猫。值得注意的是,“熊猫血”这一俗称常被泛用于所有Rh阴性血型,但严格来说,Rh阴性O型血因其双重稀缺性,是“熊猫血中的熊猫血”。
遗传与分布:地域与种族的差异密码
Rh阴性血型的遗传遵循隐性规律。若父母双方均为Rh阴性(dd基因型),子女必然为Rh阴性;若一方为显性(Dd),则有50%概率遗传阴性基因。全球范围内,Rh阴性的分布呈现显著差异:白种人占比约15%,非洲裔约5%-8%,而亚洲人群普遍低于1%。在中国,新疆地区Rh阴性比例最高(9.9‰),广西最低(1.82‰),民族差异同样明显——苗族Rh阴性比例高达13%,而汉族仅0.3%。
O型Rh阴性血的稀缺性则源于ABO与Rh系统的双重筛选。以中国汉族为例,O型人群约占40%,结合0.3%的Rh阴性比例,理论上O型Rh阴性仅占0.12%。而实际献血数据显示,某市300万献血者中仅3300人为Rh阴性,其中O型占比更低。这种地域与基因的叠加效应,使得匹配血源如同大海捞针。
临床意义:输血与生育的双重挑战
Rh阴性血型者在临床上面临特殊风险。输血安全方面,若输入Rh阳性血液,可能引发免疫系统产生抗-D抗体,导致溶血反应,严重时可致命。Rh阴性患者原则上需输注同型血液,紧急情况下可经严格配型后输注Rh阳性血,但可能引发未来输血限制。生育风险更为严峻:Rh阴性孕妇若怀有Rh阳性胎儿,首胎可能因母婴血型不合引发抗体,次胎发生新生儿溶血症的概率高达60%,需通过产前抗体筛查和免疫球蛋白注射干预。
以深圳某案例为例,一名骨科患者因抗-Fya抗体无法匹配常规血液,最终通过全国协作才找到Fya抗原阴性供血者。这类案例凸显稀有血型救治的复杂性。而宁夏曾出现一例“Rh缺失型D--”患者,其血液配型成功率趋近于零,最终依靠亲属定向献血解决危机,进一步印证建立稀有血型库的必要性。
社会支持:生命网络的共建之路
面对稀有血型群体需求,全球已建立多级响应机制。中国自2001年启动稀有血型库,并依托红十字会成立“稀有血型之家”,通过志愿者登记实现互助救援。深圳等地推行冰冻红细胞技术,将Rh阴性血液在-65℃下保存十年,提升应急储备能力。民间组织如“中国稀有血型联盟”则倡导理性救助,通过资料核验避免资源浪费,并鼓励直系亲属定向献血。
技术进步也为稀有血型管理提供新思路。基因检测可精准识别D抗原变异体,避免传统血清学检测的漏诊风险。自体输血技术在择期手术中的应用,既能规避配型难题,又可减少同种免疫风险。针对非洲裔Fya抗原阴性比例高的特点,跨国血液调配机制正在探索中。
未来展望:从应急到预防的转型
稀有血型研究仍存在诸多空白。基因编辑技术能否修正D抗原缺失?2019年《自然》杂志报道的CRISPR-Cas9修复β地中海贫血基因的案例,为Rh阴性治疗提供想象空间。血型分布与疾病易感性的关联需深入探索,例如弓形虫感染是否与Rh阴性认知行为相关,仍需大样本验证。
政策层面,建议将Rh血型检测纳入婚检和孕检项目,通过早期干预降低生育风险。可借鉴法国“全民血型数据库”经验,利用区块链技术建立动态血源网络。公众教育也需加强——调查显示,仅38%的Rh阴性者知晓自身血型特殊性,普及血型知识任重道远。

A型Rh阴性血型与Rh阴性O型血的特殊性,既是生命多样性的体现,也是医学的考题。从个体而言,知晓自身血型并参与献血登记,是对生命的双重守护;从社会视角,完善血库建设、推动科研创新,方能织就更紧密的生命安全网。未来,随着基因技术的突破和全球协作的深化,稀有血型或将不再成为医疗救治的“阿喀琉斯之踵”,而是人类共同书写的生命奇迹。