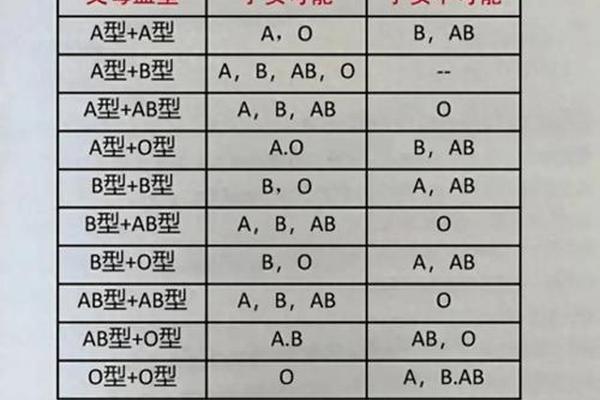
在人类ABO血型系统中,A型与B型血父母可能孕育出A型、B型、AB型或O型血的后代。近年来,多项研究提示血型与癌症风险存在统计学关联,其中O型血人群的总体患癌风险相对较低。这种潜在联系引发了公众对血型遗传与健康管理的关注。本文将从血型遗传机制、各血型癌症风险的实证研究、生物学机制假设及健康管理建议等角度,深入探讨这一交叉领域的科学发现。
血型遗传的生物学基础
根据孟德尔遗传定律,A型和B型血父母携带的等位基因组合可能产生四种血型后代。由于A和B为显性基因,O为隐性基因,父母若分别携带AO和BO基因型,其子女有25%概率为OO型(即O型血)。这种遗传多样性为研究血型与疾病关联提供了天然实验模型。
值得注意的是,血型抗原不仅存在于红细胞表面,还在消化系统、呼吸系统等上皮细胞中表达。研究发现,这些抗原可能通过调控细胞信号传导或免疫识别机制影响疾病进程。例如,O型血缺乏A/B抗原,但其血浆中含有抗A和抗B抗体,这种独特的免疫特性可能成为影响癌症易感性的关键因素。
各血型癌症风险的实证研究
O型血的低风险优势
上海交通大学团队对1.8万名志愿者25年的随访发现,O型血人群总体患癌风险比非O型血降低16%,尤其在癌(风险降低25%)、卵巢癌(24%)和胃癌(16%)中表现显著。欧洲肿瘤研究所对1.5万例患者的分析进一步证实,O型血人群外分泌腺癌风险降低20-47%。这种保护效应可能源于O型血特有的抗A/B抗体对肿瘤抗原的交叉识别作用。
B型血的相对安全性
同一研究显示,B型血人群消化系统肿瘤风险最低,胃癌和结直肠癌发病率分别比A型血降低25%和22%。在膀胱癌领域,B型血男性患病风险显著低于其他血型。但需注意,B型血女性乳腺癌风险可能存在轻微升高趋势,提示血型与癌症关联具有组织特异性。
A型与AB型血的特殊风险
A型血人群消化道肿瘤风险比非A型血增加12%,胃癌和癌风险分别升高18%和23%。AB型血则呈现矛盾特征:其肝癌风险比非AB型高42%,但癌风险比A型血低17%。这种差异可能与不同器官中血型抗原分布密度相关,例如肝细胞表面AB抗原可能影响免疫监视效率。
潜在作用机制的生物学解释
免疫监视假说
O型血个体同时携带抗A和抗B抗体的特性,可能增强对表达类似抗原的癌细胞的清除能力。研究显示,约15%的胃癌细胞表面存在类A抗原,O型血中的天然抗体可能通过抗体依赖性细胞毒性作用抑制肿瘤生长。这种机制在解释O型血癌低风险时尤为突出,因导管细胞常异常表达ABO抗原。

炎症反应调控理论
慢性炎症是癌症发生的重要诱因。A型血人群的IL-6、CRP等促炎因子基线水平较高,可能通过激活NF-κB通路促进肿瘤微环境形成。而O型血的某些基因多态性(如FUT2非分泌型)可减少肠道菌群诱导的慢性炎症,从而降低结直肠癌风险。
健康管理策略与未来展望
尽管血型提供了一定的风险提示,但环境因素仍占癌症成因的80%以上。建议不同血型人群采取针对性筛查:A型血加强胃肠镜监测,AB型血重视肝脏超声检查,O型血则需注意凝血功能异常相关的癌症类型。限酒、控制幽门螺杆菌感染等普适性措施对所有血型均具保护作用。
未来研究需在三个方向突破:一是建立百万级人群队列,结合基因组学解析血型抗原的分子机制;二是开发血型特异性生物标志物,优化早期筛查方案;三是探索血型抗原在免疫治疗中的调控作用,例如利用天然抗体增强PD-1抑制剂疗效。只有将遗传信息转化为临床实践,才能真正实现精准癌症预防。
血型与癌症风险的关联研究揭示了人类遗传多样性与疾病易感性的复杂互动。虽然O型血展现出一定保护效应,但个体健康始终是遗传背景、生活方式和环境暴露共同作用的结果。科学界需避免对血型风险的过度解读,而公众更应关注可控危险因素的干预。随着分子机制的阐明,未来或将诞生基于血型特征的新型防癌策略,为人类战胜癌症提供全新视角。