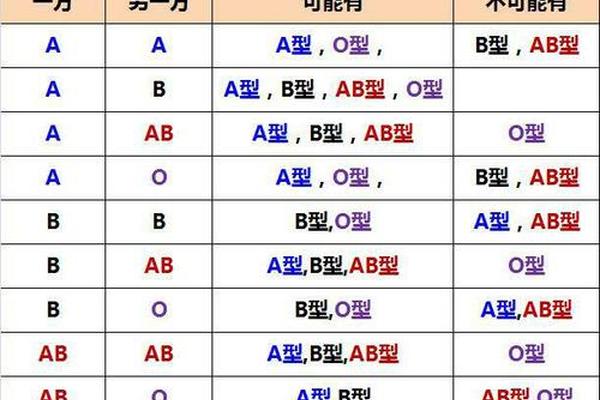
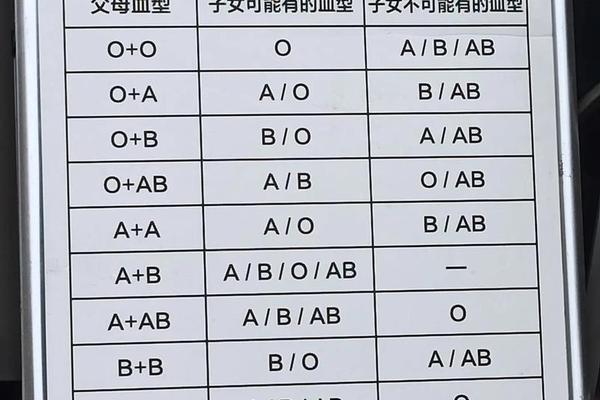
在医学检验和临床输血中,ABO血型系统的鉴定是基础且关键的一环。当血型诊断为"A型"时,意味着个体的红细胞表面存在A抗原,而血浆中则含有抗B抗体。这一结果看似简单,但其背后的抗原结构、遗传机制以及临床意义却涉及复杂的生物学原理和医学实践。A型血不仅是人类最常见的血型之一(约占全球人口的34%),其亚型差异和抗原表达的特殊性更对输血安全、器官移植和疾病研究产生深远影响。
抗原结构与分类依据
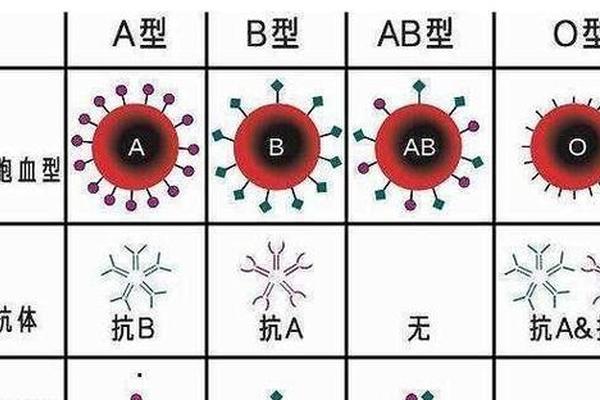
A型血的核心特征在于红细胞膜上的A型抗原。这种抗原本质是糖脂分子,由N-乙酰半乳糖胺通过α-1,3糖苷键连接在H抗原的β-D-半乳糖末端形成。H抗原本身由FUT1基因编码的岩藻糖转移酶催化产生,是ABO抗原形成的基础结构。在A型个体中,ABO基因座上的A等位基因编码α-1,3-N-乙酰氨基半乳糖转移酶,这种酶能够特异性修饰H抗原,最终形成具有免疫原性的A抗原。
抗原的表达强度直接影响血型鉴定的准确性。研究表明,A型红细胞表面的抗原密度约为8.1×10^5个/细胞,显著高于B型抗原的表达量。这种差异导致A型抗原的免疫原性更强,在输血反应中更易引发溶血现象。值得注意的是,A型抗原不仅存在于红细胞表面,还广泛分布于唾液、等体液以及上皮细胞中,这种多组织表达特性使其在器官移植配型和法医学鉴定中具有特殊价值。
遗传机制与分子基础
A型血的遗传遵循孟德尔显性遗传规律。ABO基因位于人类第9号染色体长臂(9q34.2),包含7个外显子,其中第6、7外显子编码关键的糖基转移酶功能域。当个体携带至少一个A等位基因(IA)时,红细胞即可表达A抗原。基因型为IAIA的纯合子与IAi的杂合子均表现为A型血,但两者在抗原表达量上存在差异——纯合子个体的A抗原密度比杂合子高约30%。
近年来的基因组学研究揭示了A型血亚型的分子机制。例如A1和A2亚型的差异源于ABO基因第7外显子的单核苷酸突变(c.467C>T),该突变导致酶蛋白第156位脯氨酸被亮氨酸取代,显著降低酶的催化效率。这种分子层面的差异使得A2型红细胞的A抗原数量仅为A1型的25%-30%,在血型鉴定中易被误判为O型。统计显示,我国汉族人群中A2亚型仅占A型人群的0.9%-1.5%,但在白种人中这一比例可达20%。
临床意义与输血安全

在输血医学中,A型血的准确鉴定关乎生命安危。根据免疫学原理,A型受血者只能接受A型或O型血液,因其血浆中的抗B抗体会攻击B型或AB型红细胞。但实际临床中需特别注意亚型问题:当A2型患者输入A1型血液时,约2%的个体会因血浆中存在抗A1抗体而发生迟发性溶血反应。现代血库对A型血的亚型检测已成为常规流程,尤其对反复输血患者需采用试管法或凝胶微柱法进行精细分型。
在产科领域,A型血的特殊性同样值得关注。若O型血母亲怀有A型胎儿,母体产生的IgG型抗A抗体可通过胎盘引发新生儿溶血病。数据显示,约20%的O型孕妇会产生临床意义的抗体效价,其中0.3%-2%会导致需要治疗的新生儿溶血。通过产前抗体筛查和孕期监测,这类并发症的检出率已提升至95%以上,显著降低了围产期风险。
亚型差异与检测挑战
A型血内部的亚型多样性给临床检测带来特殊挑战。除常见的A1和A2亚型外,还存在A3、Ax、Am等罕见变异型,这些亚型的共同特征是A抗原表达量显著降低或空间构象异常。例如Ax型红细胞仅能通过抗人球蛋白试验检测到微弱反应,常规玻片法极易误判为O型。统计显示,我国每年因A型亚型误判导致的输血事故约占所有血型相关医疗差错的12%。
针对这些挑战,国际输血协会推荐三级检测体系:初筛采用玻片法,可疑样本使用试管法增强敏感性,最终通过分子生物学方法(如PCR-SSP)确认基因型。最新研究显示,基于单克隆抗体的流式细胞术可将A亚型检测灵敏度提升至99.7%,同时将检测时间缩短至30分钟,这为临床快速精准分型提供了新方向。
A型血的生物学特性深刻影响着现代医学实践。从抗原表位的分子结构到基因多态性的临床表达,从基础输血安全到复杂疾病关联,这一血型系统的研究始终推动着精准医学的发展。随着二代测序技术的普及,未来血型鉴定将趋向基因层面分析,不仅能更准确识别稀有亚型,还可预测个体对特定疾病的易感性。建议医疗机构加强A亚型检测能力建设,同时开展公众科普教育,使血型知识真正服务于个体化医疗和健康管理。
现有研究仍存在若干空白领域:例如A抗原在肿瘤免疫中的作用机制尚未完全阐明;不同A亚型人群对传染病的易感性差异缺乏大规模队列研究。这些问题的突破将有助于开发新型治疗策略,使血型研究从传统的输血医学向更广阔的精准医疗领域延伸。