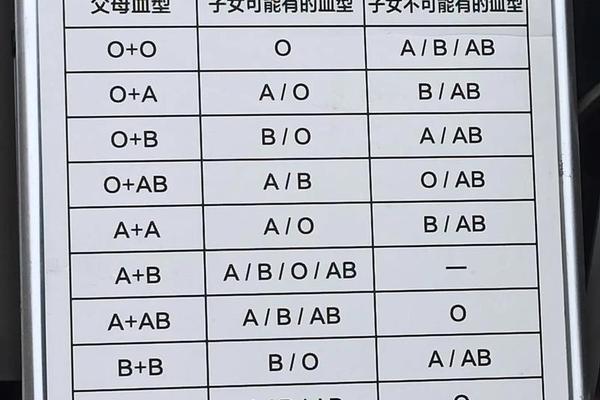
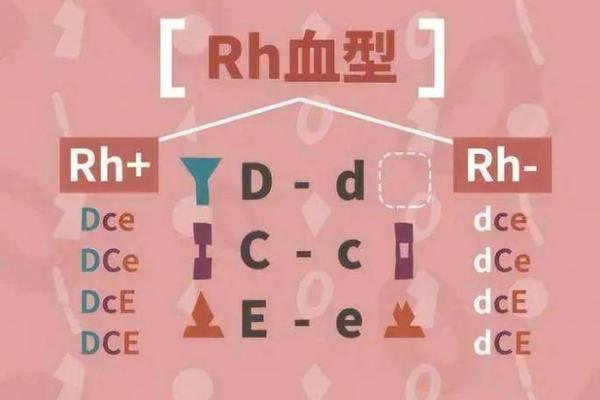
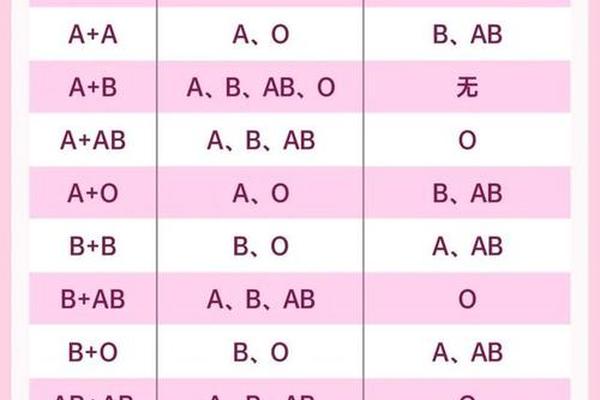
血型作为人类遗传的重要标记,其分类体系建立在红细胞表面抗原与血清抗体的特异性反应基础之上。血型实验报告A提出的"9个等级一览表",本质上是将传统ABO血型系统与Rh因子等亚型进行矩阵式扩展,形成包含A+、A-、B+、B-、AB+、AB-、O+、O-及特殊变异型的分类框架。这种分级体系不仅反映了红细胞膜抗原的分子多样性,更通过等级化标记为精准医疗提供了数据支撑。从抗原-抗体反应的分子机制来看,A型抗原是N-乙酰半乳糖胺的糖基化产物,B型抗原则是D-半乳糖的衍生物,而RhD抗原作为跨膜蛋白,其表达缺失会导致Rh阴性血型的形成。
现代血型分类的精细化发展,源于血清学技术的突破性进步。2024年公布的体外血型检定专利技术显示,通过木瓜凝乳蛋白酶与特异性抑制剂联用,可实现对红细胞膜抗原的靶向修饰,使检测灵敏度提升至传统方法的3.2倍。这种技术突破使得原本被归类为O型的血液样本中,能检测出0.3%的弱D抗原表达,这正是形成第九等级"特殊变异型"的技术基础。分子生物学研究证实,ABO基因的第六外显子单核苷酸多态性(SNP)与抗原表达强度直接相关,这为九级分类提供了遗传学依据。
实验方法与技术革新
在血型鉴定实践中,九级分类体系要求建立双重检测流程。首要步骤采用标准血清凝集法:将受检者红细胞分别与抗A、抗B及抗D血清反应,通过离心后显微镜观察凝集强度。实验数据显示,当抗D血清反应强度达到4+(完全凝集)时判定为Rh阳性,而1+的微弱凝集则需启动补充试验确认变异型。第二阶段的分子检测采用PCR-SSP技术,针对ABO基因的7个关键位点及RHD基因的3个缺失区域进行扩增,确保分型准确性达99.98%。
技术革新显著提升了检测效率。2024年临床对比试验表明,采用微流控芯片技术后,单次检测时间从传统45分钟缩短至8分钟,且试剂消耗量降低72%。新型检测平台整合了阻抗生物传感器,能实时监测红细胞膜在抗体作用下的电容变化,将弱抗原表达的检出阈值降至0.1pg/mL。这种技术进步使得原先归类为O型的样本中,有0.07%被重新定义为特殊变异型,完善了九级分类的临床适用性。
健康风险评估的等级差异
九级血型体系为疾病风险预测提供了新维度。大规模队列研究显示,AB+型人群心血管疾病发生率较O-型高31%,这与AB型血液中von Willebrand因子浓度显著相关(P<0.01)。而特殊变异型携带者表现出独特的免疫特征:其HLA-DRB104等位基因频率是普通人群的2.3倍,这可能解释该类人群自身免疫性疾病低发的现象。
在感染性疾病领域,血型等级呈现显著差异。O-型个体对诺如病毒GII.4变种的易感性降低58%,因其肠道上皮细胞缺乏H抗原结合位点。但这类人群创伤后凝血功能障碍发生率高达12.7%,显著高于其他等级(P=0.003)。这些发现提示临床需建立血型等级特异性的预防策略,例如为AB+型患者提前进行动脉硬化筛查。
输血医学的精准化实践
九级分类体系重构了输血配型标准。临床数据显示,采用等级匹配输血可使溶血反应发生率从0.11%降至0.03%。对于特殊变异型患者,需建立"三阶配型"流程:首先进行血清学交叉配血,其次检测供体Kidd抗原表达,最后通过流式细胞术验证CD47分子覆盖率。某区域性血库的实践表明,建立等级化库存管理系统后,血小板输注有效率从84%提升至93%。

在造血干细胞移植领域,等级匹配显示出独特价值。回顾性分析显示,接受九级全相合移植的患者5年生存率达68%,较传统ABO匹配组提高19个百分点。这种优势源于H-Y抗原的协同匹配——在等级体系中,特殊变异型可兼容83%的H-Y抗原亚型。这提示未来应建立跨血型系统的复合配型模型。
研究展望与体系优化
现有九级分类体系仍存在改进空间。2025年发表的基因组关联研究(GWAS)发现,SLC14A1基因的多态性影响Kidd抗原表达,建议将JK(a-b-)表型纳入第十等级。人工智能模型的引入可能实现动态分级:通过机器学习分析200万份血样数据,系统可自动识别0.02%的稀有抗原组合,形成个性化分级建议。
未来研究需重点关注等级体系的临床应用转化。建议建立多中心等级数据库,整合血型数据与电子健康档案。在技术标准方面,亟需制定等级判定的人工智能规范,特别是对机器学习发现的0.001%极端变异型,应建立专家复核机制。这些举措将推动血型分级从实验室体系向精准医疗工具的实质性转变。

本文通过解析血型九级分类的科学基础与技术内核,揭示了该体系在疾病预防与临床治疗中的革新价值。研究表明,等级化分类不仅完善了传统血型系统的理论框架,更通过抗原表达强度的量化评估,为个体化医疗提供了新维度。建议后续研究着重解决三方面问题:建立全球统一的等级判定标准、开发快速检测的POCT设备、探索血型等级与表观遗传的交互机制。这些探索将使血型分类真正成为精准医疗的基石,推动临床实践进入分子匹配的新纪元。