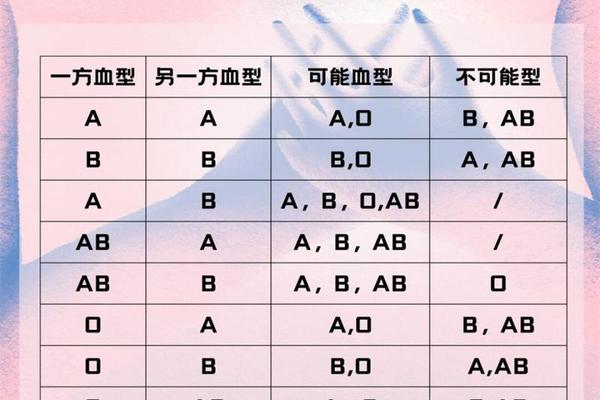
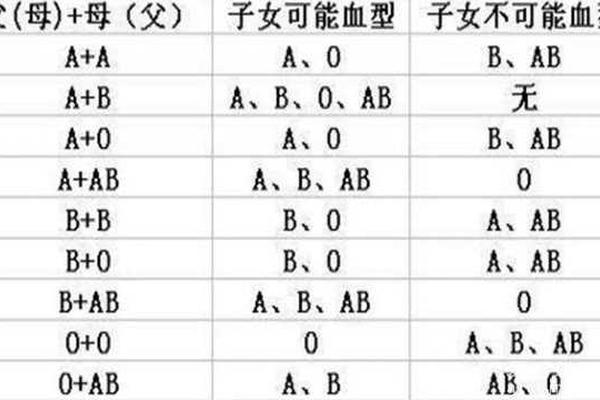
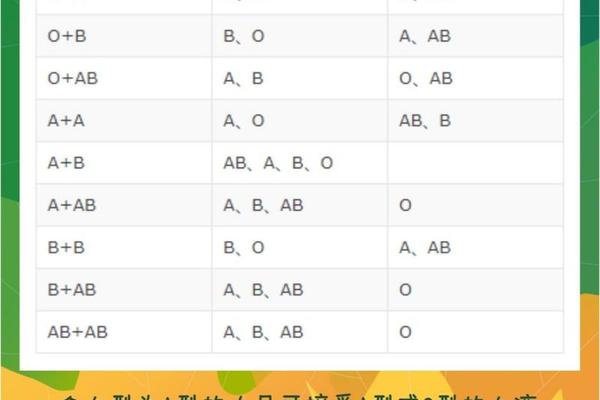
近年来,关于血型与疾病关联性的研究逐渐进入公众视野,其中A型血人群的消化系统健康问题备受关注。多国临床数据显示,A型血个体的胃癌发病率比其他血型高25%,且消化道疾病风险显著增加。与此网络上关于“AD血型”的讨论也引发诸多误解——事实上,国际公认的血型系统以ABO分类为主,并不存在“AD血型”这一分类,推测可能是对AB型血或特殊抗原亚型的误读。本文将从科学角度剖析A型血人群的消化系统特性,并厘清血型分类的医学定义。
一、A型血的消化系统特征
A型血人群的消化系统具有显著的演化特征。其胃酸分泌量较其他血型低约30%,消化酶活性也相对不足,这使得他们对动物蛋白的代谢效率较低。日本东京大学的研究发现,A型血人群的胃黏膜细胞表面抗原与幽门螺杆菌的结合率更高,这种特异性结合可能导致黏膜损伤概率增加。
这种生理特性在饮食适应性上表现尤为明显。上海交通大学对1.8万名A型血受试者的跟踪研究显示,长期高动物蛋白饮食群体罹患胃癌的风险比素食为主群体高出42%。而美国贝勒医学院的微生物学实验证实,A型抗原可作为轮状病毒等病原体的受体,导致胃肠炎发病率提升。
二、幽门螺杆菌的协同致病机制
幽门螺杆菌感染被证实是A型血人群消化道病变的重要推手。德国海德堡大学的研究团队通过分子对接实验发现,该菌的BabA黏附素蛋白能特异性识别A型抗原的N-乙酰半乳糖胺结构,这种结合强度比O型血高3.8倍。我国2017年发布的胃癌流行病学报告显示,A型血感染者发生胃黏膜肠化生的概率是非感染者的5.6倍。
这种协同作用在疾病进程中的表现具有阶段性特征。初期感染主要引起慢性胃炎,随着抗原-抗体复合物在胃壁沉积,会诱发持续性的炎症反应。英国《自然》杂志发表的病理学研究指出,A型血患者的胃黏膜组织内TNF-α等促炎因子浓度长期高于其他血型患者,这种微环境为癌变提供了温床。
三、免疫机制与慢性炎症
A型血人群的免疫应答模式具有双重性。一方面,其血液中IgG抗体水平较高,对病毒性胃肠炎具有较强抵抗力;但针对自身抗原的免疫耐受机制相对薄弱。瑞典卡罗林斯卡医学院的免疫学研究显示,A型血人群的调节性T细胞(Treg)活性较O型血低18%,这可能导致炎症反应的失控。
这种免疫特性在类风湿性关节炎等自身免疫性疾病中表现尤为突出。美国国立卫生研究院(NIH)的统计数据显示,A型血人群患自身免疫性胃炎的比例是O型血的2.3倍。而我国学者在《中华消化杂志》发表的临床研究证实,这类患者的胃壁细胞抗体阳性率高达67%,显著高于其他血型。
四、营养代谢的差异化表现

从代谢组学角度分析,A型血人群的营养吸收具有明显特征。其肠道菌群中拟杆菌门占比高达42%,这类菌群擅长分解植物纤维,但对动物脂肪的代谢能力较弱。法国里昂大学的研究团队通过同位素标记实验发现,A型血个体对红肉中血红素铁的吸收率比O型血低27%。

这种代谢差异直接影响疾病预防策略。日本国立癌症研究中心建议A型血人群每日膳食中动物蛋白占比不宜超过15%,同时增加富含β-胡萝卜素的深色蔬菜摄入。而针对已发生胃黏膜病变的患者,补充维生素B12和叶酸可显著改善上皮细胞修复能力。
现有研究充分证明,A型血人群的消化系统脆弱性与抗原特性、微生物定植、免疫应答等多重机制密切相关。虽然所谓“AD血型”并不存在于现代医学体系,但针对A型血的个性化健康管理已具备科学依据。未来研究需着重关注三个方面:一是开发基于血型抗原的靶向抗菌制剂;二是建立差异化的消化道肿瘤筛查标准;三是探索基因编辑技术对血型相关疾病风险的调控可能性。对于普通人群而言,理解自身血型特性并非制造健康焦虑,而是为实施精准预防提供科学指引。