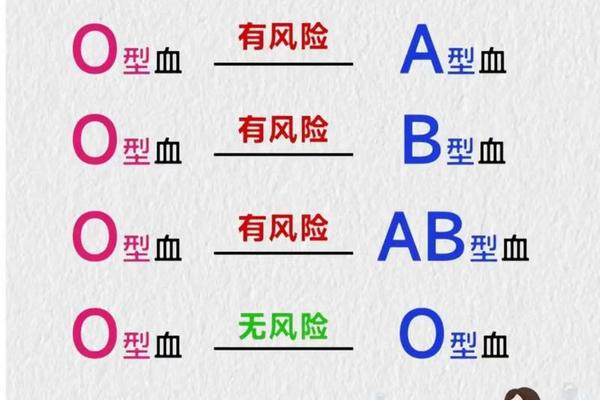
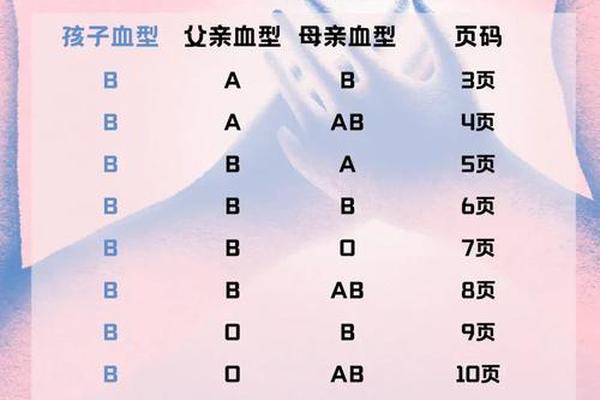
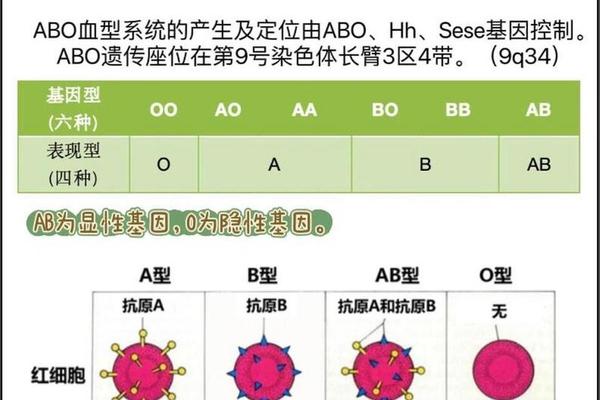
血型是人类遗传特征的重要标识,由红细胞表面的抗原决定。ABO血型系统将血液分为A、B、AB、O四类,而Rh血型系统则根据红细胞是否携带D抗原分为Rh阳性和Rh阴性。母亲若为"A型阴性血型",意味着她的ABO血型为A型(红细胞携带A抗原),同时Rh血型为阴性(缺乏D抗原)。这种组合在人群中较为特殊,因为A型血约占全球人口的35%,而Rh阴性血仅占1%左右。
A型阳性与阴性的核心差异在于D抗原的存在与否。Rh阳性个体的基因型为DD或Dd,而Rh阴性则为dd。若母亲的基因型为dd,其子代只能从父母各获得一个d基因,因此无论父亲的血型如何,孩子至少有50%的概率遗传到d基因。若父亲携带隐性d基因(如Dd),孩子甚至可能完全遗传dd基因型,成为Rh阴性血型。这种遗传特性使得Rh阴性血型具有隐性遗传的特点,即使父母表现型为Rh阳性,仍可能生育Rh阴性后代。
孕期风险与新生儿溶血
Rh阴性血型母亲若怀有Rh阳性胎儿,可能引发母婴血型不合溶血病。当胎儿的Rh阳性红细胞通过胎盘进入母体血液循环时,母体会产生抗D抗体。首次妊娠时,抗体效价较低,通常不会对胎儿造成严重伤害;但第二次妊娠若胎儿仍为Rh阳性,母体的记忆性免疫反应会迅速增强,抗体通过胎盘攻击胎儿红细胞,导致溶血性贫血、黄疸甚至胎死宫内。
临床数据显示,约13%的Rh阴性孕妇在未接受预防措施的情况下,会在第二胎出现严重溶血反应。为降低风险,医学界建议Rh阴性母亲在妊娠28周及产后72小时内注射抗D免疫球蛋白,以中和进入母体的胎儿红细胞,阻断抗体产生。例如,2021年北京妇产医院的研究表明,规范使用免疫球蛋白可使Rh溶血病的发生率从15%降至1%以下。
输血安全与应急管理
Rh阴性血型者面临输血资源稀缺的挑战。由于仅占人口的1%,紧急情况下可能难以及时获得匹配血液。根据中国血液中心的统计数据,Rh阴性血库的日常储备量仅为需求量的30%。Rh阴性个体需提前在区域性"熊猫血库"登记,并与医疗机构建立应急联系机制。
输血时必须严格遵守同型输注原则。若Rh阴性者误输Rh阳性血,首次输血可能引发轻度溶血反应,而二次输血将导致致命性急性溶血。特殊情况下(如大出血抢救),O型Rh阴性血可作为"万能供血者"暂时使用,但需去除血浆中的抗A抗体以避免不良反应。
遗传咨询与家庭规划
对于计划生育的Rh阴性女性,基因检测可提前评估风险。若配偶为Rh阳性,可通过绒毛膜取样或游离DNA检测确定胎儿Rh血型。2024年深圳生殖医学中心的研究显示,非侵入性产前检测(NIPT)对胎儿Rh血型的判断准确率达99.3%。若胎儿为Rh阳性,建议加强孕期抗体滴度监测,每4周检测一次,孕晚期缩短至每2周一次。
对于已产生抗体的孕妇,可采取血浆置换、宫内输血等干预措施。例如,武汉大学中南医院的案例表明,孕20周开始每月一次宫内输血,可显著改善胎儿贫血状况,延长妊娠周期至34周以上。

社会支持与医学进展
全球已建立多个Rh阴性互助组织,如国际熊猫血协会(IPBS)通过区块链技术实现实时血源匹配。基因编辑技术为根治Rh溶血病带来新希望,2023年《自然·医学》期刊报道,CRISPR-Cas9技术成功修饰造血干细胞中的RhD基因,使其表达D抗原,从而避免免疫攻击。人工合成血研究取得突破,2024年英国NHS已开展实验室培育Rh阴性红细胞的临床试验。
母亲A型阴性血型的特殊性与风险性,本质上是ABO与Rh血型系统叠加作用的结果。通过规范产前管理、完善输血体系、发展基因技术,可显著提升这类人群的生育安全与生存质量。未来研究需重点关注三方面:一是开发更精准的抗体检测技术,实现溶血风险的早期预警;二是扩大人造血技术的应用范围,彻底解决血源短缺问题;三是探索表观遗传学干预手段,从基因表达层面调控抗原呈递机制。建议所有Rh阴性女性孕前进行系统咨询,并积极参与稀有血型互助网络,将个体风险转化为群体共济的医学资源。