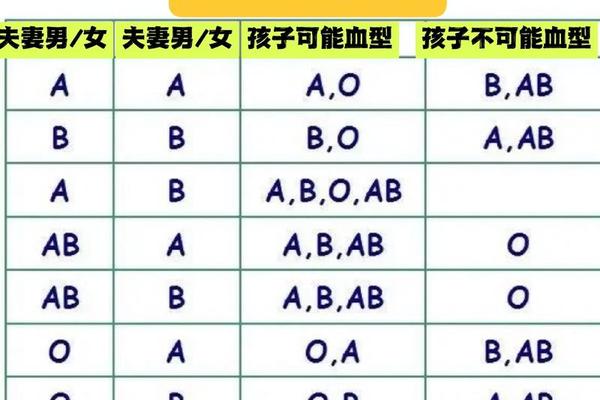
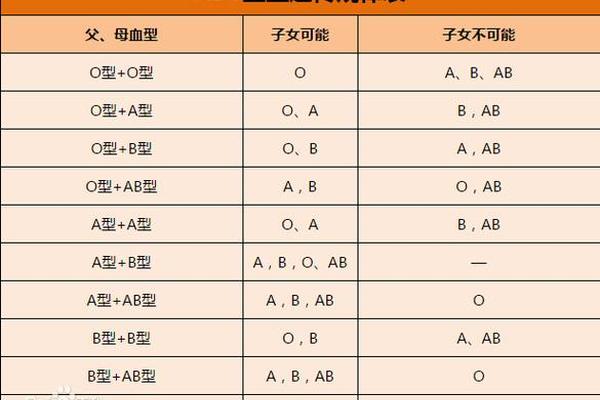
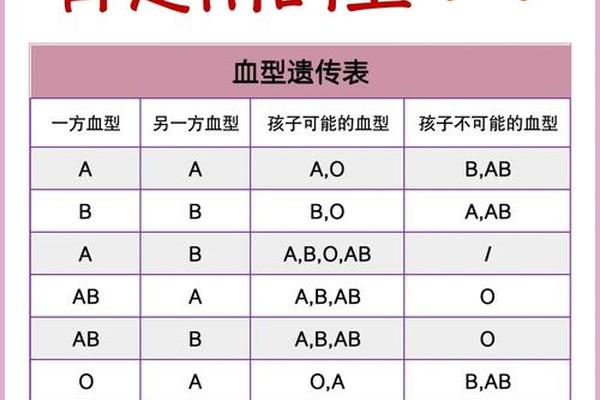
ABO血型系统与Rh血型系统是临床输血中最重要的两大分类标准。ABO系统根据红细胞表面A、B抗原的有无分为A、B、AB、O四型,而Rh系统则以D抗原的存在与否划分Rh阳性(+)或阴性(-)。A+血型实质是ABO系统中的A型叠加Rh阳性特征,这与单纯ABO系统的A型血存在本质差异。在遗传学层面,ABO基因位于9号染色体,RhD基因则位于1号染色体,两者属于独立遗传的血型系统。

现代医学研究发现,ABO系统中的A型血存在多个亚型,其中A1和A2占所有A型血的99.9%以上。A1型红细胞同时携带A和A1抗原,而A2型仅表达A抗原。这种差异源于A1转移酶能将H抗原完全转化为A抗原,而A2转移酶活性较弱,导致A2型红细胞表面残留更多H抗原。Rh系统方面,D抗原的表达受RHD基因调控,基因缺失或突变会导致Rh阴性表型,我国汉族人群中Rh阴性比例不足0.3%。
血清学鉴定的技术路径
传统血清学检测是血型分型的金标准。对于ABO亚型,试管法通过观察抗A血清与红细胞的凝集强度进行判别:A1型与抗A反应呈4+凝集,A2型则为2+,而Ax型可能仅出现微弱凝集或混合视野现象。Rh血型检测则需使用抗D试剂,阳性样本出现明显凝集,阴性样本无反应。值得注意的是,约0.2%的弱D表型需通过增强试验(如抗人球蛋白试验)才能准确判定。
玻片法作为快速筛查手段,在急诊输血中具有应用价值。但研究发现,其对A亚型的漏检率达15%,主要因抗原表达过弱导致肉眼判读困难。国际血液学标准化委员会建议将微柱凝胶法作为补充,该方法利用葡聚糖分子筛分离游离与凝集细胞,可将A3亚型的检出灵敏度提升至98%。
分子生物学的革新突破
基因测序技术为复杂血型鉴定提供了新方案。PCR-SSP法可特异性扩增ABO基因的第6、7外显子,准确识别A1(261G缺失)和A2(467C>T)的基因特征。北京地区的分子流行病学研究显示,A102等位基因占当地A型人群的89.7%,而A201等位基因仅0.03%。对于Rh系统,多重连接探针扩增技术(MLPA)能检测RHD基因的全长缺失,对Rh阴性判定的准确性达99.99%。

近年来,微流体芯片技术实现了ABO与Rh系统的同步检测。浙江大学附属医院的研究表明,该技术对Ax亚型的检测时间缩短至2小时,且能同时分析35个SNP位点,尤其适用于移植后血型嵌合体的鉴定。但成本较高限制了其在基层医院的普及,目前主要应用于疑难血型鉴定和法医学领域。
临床输血的策略调整
A亚型患者的输血需遵循特殊原则。A2型个体血清中可能含有抗A1抗体,输注A1型红细胞可能引发溶血反应。上海血液中心的指导方案建议:A2患者应优先输注A2或O型洗涤红细胞,血浆选择需交叉配型。对于Rh阴性患者,除紧急情况外必须输注Rh阴性血液。但研究发现,Rh阳性红细胞输注给Rh阴性患者后,约20%会产生抗D抗体,因此育龄期女性需严格遵循阴性输血原则。
在稀有血型管理方面,南京儿童医院建立了包含217例Ax亚型的冷冻血库,采用甘油化冷冻技术使红细胞保存期延长至10年。对于cisAB型等罕见血型,推荐采用自体输血或亲属定向捐献模式。武汉协和医院的临床数据显示,采用分子分型指导的精准输血使溶血反应发生率从0.12%降至0.03%。
未来发展的研究方向
血型鉴定技术正朝着智能化方向发展。人工智能辅助判读系统已在部分三甲医院试运行,通过深度学习算法分析凝集模式,对A亚型的识别准确率可达96.5%。基因编辑技术的突破为通用血型制备带来希望,复旦大学团队利用CRISPR-Cas9敲除ABO基因,成功将A型红细胞转化为O型,转化效率达91%。
群体遗传学研究揭示,我国西南少数民族的A2亚型频率(0.8%)显著高于汉族(0.3%),这为区域性血库建设提供了数据支持。未来需建立全国性血型基因数据库,开发快速床旁检测设备,并通过合成生物学技术生产稀有血型抗原,从根本上解决血源短缺问题。
总结与建议
准确区分A型血的ABO亚型和Rh属性,是保障输血安全的核心环节。血清学方法作为基础检测手段,需与分子生物学技术形成互补。临床建议:①常规检测增加抗A1试剂和增强凝集法;②对正反定型不符样本强制进行基因分型;③建立区域性稀有血型动态监测网络。随着单细胞测序和纳米孔技术的进步,未来有望实现全自动、超快速的血型精准鉴定,为个性化输血医学开辟新路径。