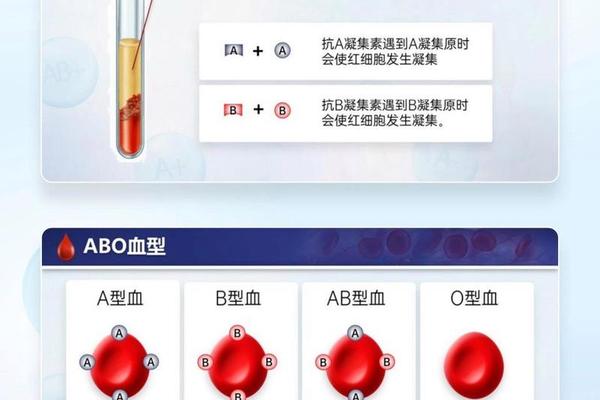
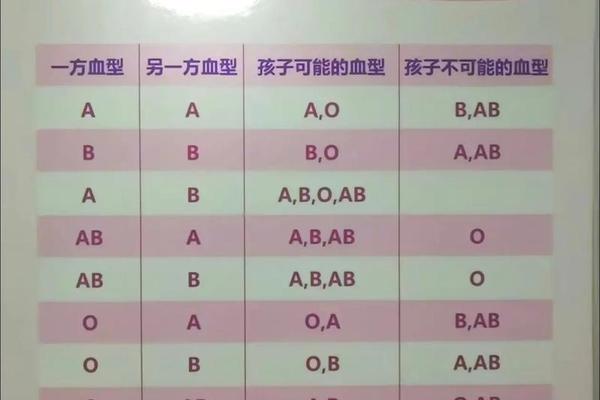
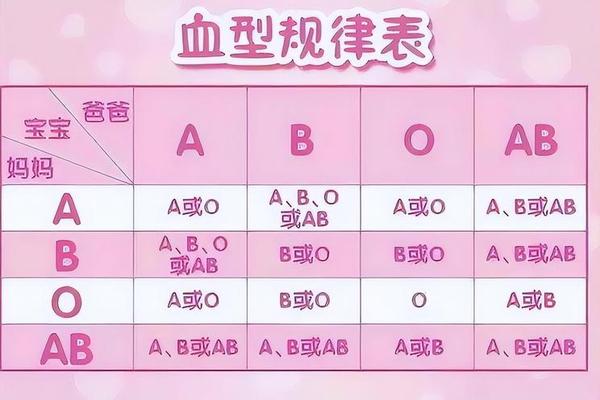
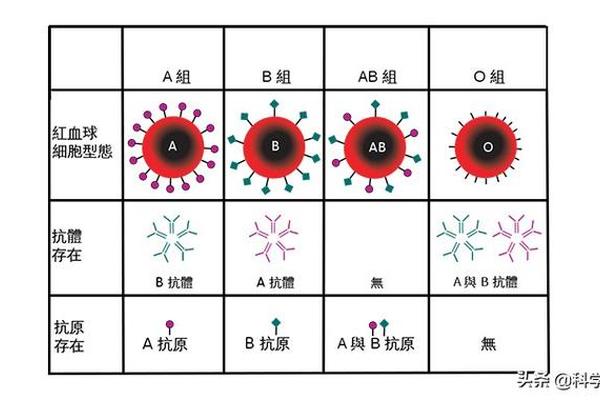
血型作为人类基因的重要表达形式,其与体质特征的关系一直是医学和营养学领域的热点。在众多血型中,A型血人群的体重管理特点尤为特殊——部分人呈现出“易瘦体质”,而另一部分则可能因代谢效率低下导致肥胖风险升高。这种矛盾现象的背后,既与基因决定的消化系统特征有关,也受到饮食结构、心理压力等多重因素的共同影响。与此B型血人群因独特的代谢机制,被认为是血型群体中最容易发胖的类型之一。
从生理机制来看,A型血的起源与早期农耕文明密切相关,其基因中保留了更多适应植物性饮食的特征。研究指出,A型血人群的胃酸分泌量相对较少,消化动物性蛋白质的效率较低,这使得他们在摄入高脂肪、高热量的肉类时更容易出现代谢负担。这种“低效”的消化特性也可能成为双刃剑——当饮食以素食为主时,A型血人群的肠道菌群更易保持平衡,从而减少脂肪囤积;反之,若长期摄入超出消化能力的食物,则会导致能量过剩。
二、饮食结构的适配性与代谢效率
A型血人群的易瘦体质与其饮食适配性存在显著关联。上海交通大学的研究显示,A型血携带者对植物性食物具有更强的代谢优势,其体内特定的酶系统能更高效地分解谷物和蔬菜中的纤维与营养素。例如,橄榄油、豆类等食物中的不饱和脂肪酸与A型血人群的胆固醇代谢路径高度契合,有助于维持血脂平衡。这种特性使得遵循素食为主的A型血人群更易保持苗条体型,而偏好西式高脂饮食者则可能因代谢滞后引发肥胖。
反观B型血人群,其基因源于游牧民族,具备强大的杂食消化能力。但这种看似“高效”的代谢系统却暗藏风险:B型血人群对碳水化合物的分解速度过快,导致血糖波动剧烈,更容易产生饥饿感,从而形成“吃得多、饿得快”的恶性循环。加拿大多伦多大学的膳食实验表明,B型血人群在摄入小麦、玉米等谷物时,胰岛素敏感性显著降低,这会促使多余糖分转化为脂肪储存。
三、心理压力与内分泌调节机制
A型血人群的体重波动与心理状态存在微妙联系。日本京都大学的研究发现,A型血携带者的皮质醇水平对外界压力更为敏感。当长期处于焦虑状态时,其肾上腺会过度分泌应激激素,进而抑制甲状腺功能,使基础代谢率下降10%-15%。这种现象解释了为何部分A型血人群在高压环境下会出现“压力性肥胖”,即便保持原有饮食结构也难以控制体重。
相比之下,B型血人群的肥胖风险更多源于生理性代谢缺陷。美国《糖尿病学》杂志的流行病学调查显示,B型血人群的瘦素抵抗发生率比其他血型高28%,这意味着他们的饱腹感信号传递效率更低。B型血特有的红细胞抗原会干扰脂肪细胞分化因子(PPARγ)的表达,导致皮下脂肪分解速率降低30%以上。
四、争议与科学研究的局限性

尽管血型与体重的关联性被部分研究所支持,但其科学严谨性仍存争议。2018年一项纳入近千名受试者的对照实验表明,当不同血型人群采用相同饮食方案时,体重变化差异并无统计学意义。这提示血型对体型的影响可能被其他混杂因素(如运动习惯、肠道菌群)所掩盖。血型抗原与代谢通路的具体作用机制尚未完全阐明,现有结论多基于观察性研究,缺乏分子层面的直接证据。
五、结论与健康管理建议
综合现有研究,A型血人群的体重特征呈现显著的两极分化:遵循植物性饮食者易维持苗条体型,而偏好高脂饮食或长期高压者则面临代谢失衡风险;B型血人群因先天代谢缺陷更易积累脂肪,需特别注意碳水化合物的摄入量与运动强度。值得注意的是,血型仅是影响体重的因素之一,个性化健康管理应结合基因检测、生活习惯等多维度数据。
未来研究需在以下方向深入探索:一是建立大规模血型-代谢组学数据库,解析不同血型人群的脂质代谢通路差异;二是开发基于血型特征的运动-营养联合干预模型;三是探究红细胞抗原与肠道菌群互作对能量代谢的影响机制。唯有打破“血型决定论”的片面认知,才能为体重管理提供更科学的解决方案。