在临床医学中,血型鉴定是输血安全的核心环节。当同一患者的血型检测结果在不同场景下出现“A型”与“B型”的矛盾时,不仅可能引发医患纠纷,更可能危及患者生命。这种看似荒诞的“血型反复”现象背后,隐藏着技术操作、疾病状态、遗传变异等多重复杂因素。从实验室误差到罕见基因突变,从疾病干扰到医疗技术进步,每一个环节都可能成为血型“身份”扑朔迷离的推手。
一、技术操作与人为失误
血型检测流程中的任何环节疏漏都可能造成结果偏差。网页58明确指出,检验者工作粗心是常见错误来源,例如试管编号错误、肉眼观察漏检弱凝集、未同步进行反定型等。某案例显示,当红细胞悬液浓度过低且未充分离心时,A型抗原的微弱凝集可能被误判为阴性,导致错误报告为B型。抗血清的误用更具隐蔽性——若将“抗-A血清”误认为A型血清,会导致抗原抗体反应方向错误,完全颠倒检测结果。
现代血型检测虽已实现半自动化,但人为因素仍不可忽视。网页76描述的网购试纸自测案例中,操作者因血量不足、缓冲液污染、超时观察等导致结果偏差,暴露出非专业检测的局限性。而网页77中医院检验科因操作流程不规范导致同一患者三年内出现O型与B型两种检测结果,更突显标准化操作的重要性。
二、样本异常与试剂干扰
血液样本的质量直接影响检测准确性。网页60提到,样本污染会产生假阳性,如腐败样本释放的细菌酶可能分解红细胞表面抗原,使A型呈现B型特征。华通胶污染在新生儿血样中尤为危险,这种脐带胶状物质会引发假性缗钱状凝集,干扰正定型结果。某些药物(如肝素)或输注异体血浆会改变血液理化性质,导致抗血清反应异常。
试剂问题同样不容小觑。抗血清效价下降是常见干扰因素:某研究显示,贮存不当的抗-A血清效价从1:128降至1:8时,对A2亚型红细胞的凝集能力完全消失,可能将A型误判为O型。网页66的研究对比微柱凝胶法与聚凝胺法,发现后者因灵敏度不足导致19例不规则抗体漏检,其中包含可能干扰ABO定型的结果。这些案例表明,试剂选择和质量控制直接影响检测系统的可靠性。
三、疾病状态下的血型异变
特定病理状态可导致血型抗原表达异常。网页58指出,高浓度冷凝集素会引起红细胞自凝,掩盖真实血型。例如,支原体肺炎患者的IgM冷凝集素效价可达1:1000以上,在室温检测时使A型红细胞呈全凝集状态,反定型却显示B型特征。血液系统疾病的影响更为深远:白血病患者的A抗原表达可能减弱至正常水平的10%,导致正定型呈弱阳性或阴性。
器官移植带来的生物学改变更具颠覆性。网页44报道的移植案例显示,供体O型干细胞成功植入A型受者后,患者血型完全转变为O型,但残留的宿主血浆仍含抗-B抗体,形成正反定型矛盾。这种生物学身份的“重塑”要求临床必须结合病史进行综合判断,单一检测结果已无法反映复杂现实。
四、特殊血型的鉴定挑战
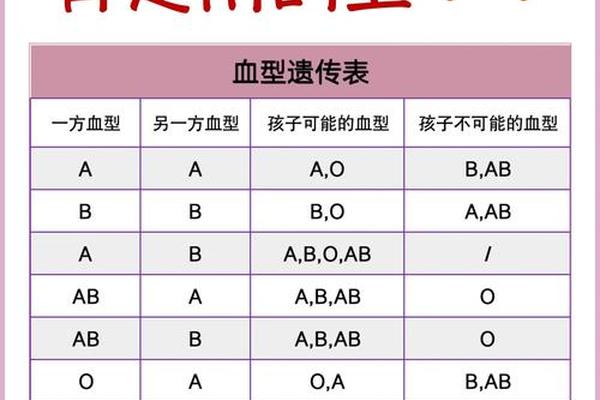
ABO血型系统的亚型是检测误差的高发区。网页24记录的AB亚型案例中,试管法显示AB型,而微柱凝胶法却判为A型,最终经基因检测确认为AB亚型。此类亚型的B抗原位点数仅为正常值的15%-25%,常规血清学检测极易漏检。更罕见的顺式AB型(cis-AB)更具迷惑性,如网页13所述案例:父亲携带AB基因同源染色体,其O型妻子可诞下AB型子女,完全打破常规遗传规律。
稀有血型系统的交叉干扰需特别关注。网页43提到的孟买型(Bombay血型)因缺乏H抗原,常规检测呈现O型特征,但血清中含强效抗-H抗体。若将此类患者误判为O型输血,可能引发致命性溶血反应。基因检测显示,这类血型的FUT1基因存在纯合突变,传统血清学方法已无法准确识别。
五、检测技术的革新方向
突破传统血清学的技术局限已成必然趋势。网页51介绍的无锡血站案例中,基因分型技术成功鉴定出2例AB亚型和2例弱D型,其通过荧光PCR直接检测ABO基因的SNP位点,避免了抗原表达减弱造成的误判。网页52报道的AI辅助试纸技术更具革命性:机器学习算法分析光谱特征,30秒内完成ABO/Rh分型,对微弱抗原的识别精度达99%。
标准化检测体系的建立迫在眉睫。网页73描述的溴甲酚绿试纸通过pH值变化实现多重血型抗原同步检测,其自动化判读系统将人为误差降至0.1%以下。这些技术进步提示,未来血型鉴定需构建“血清学+分子生物学+人工智能”的三维验证体系,特别是在急诊和基层医疗场景中,便携式基因检测设备将发挥关键作用。
血型检测的“身份困惑”本质上是生物复杂性、技术局限性与认知盲区共同作用的结果。从操作规范到试剂质控,从疾病干预到技术创新,每个环节都需要建立更精细的风险防控机制。建议临床实践中推行以下措施:①对正反定型不符者强制进行基因检测;②建立稀有血型基因数据库;③开发基于CRISPR技术的即时检测工具。唯有将技术革新与临床认知同步提升,才能终结血型检测的“罗生门”,为输血安全筑起真正的生命防线。