在人类复杂的血型系统中,ABO与Rh血型的双重分类构成了临床医学的基石。A型Rh阴性血作为其中的特殊存在,既是ABO系统中的A型血,又属于Rh血型系统中的阴性群体。这种双重属性使其在输血医学和遗传学领域具有独特的研究价值。根据ABO血型分类,A型血的红细胞表面携带A抗原,血浆中含有抗B抗体;而Rh血型则以D抗原的存在与否为判定标准,Rh阴性个体的红细胞缺乏D抗原,其全球分布呈现显著的地域差异。
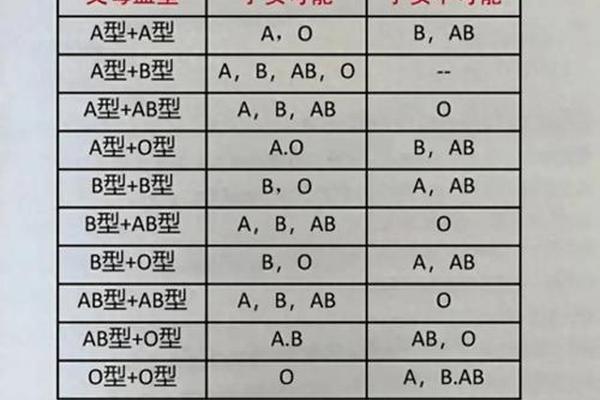
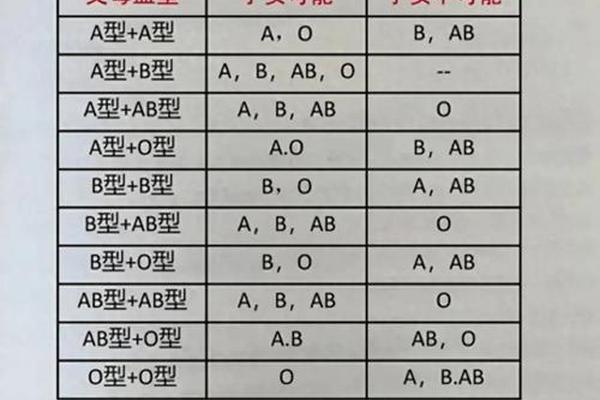
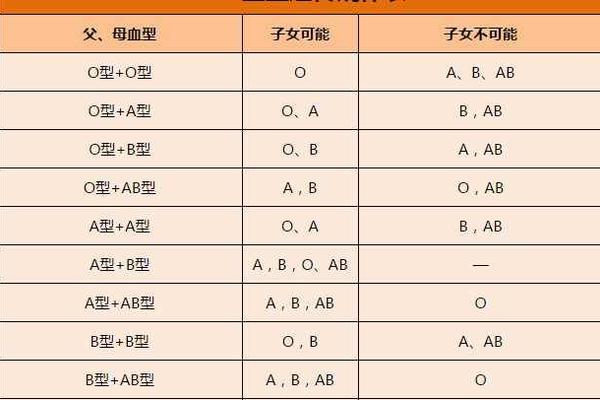
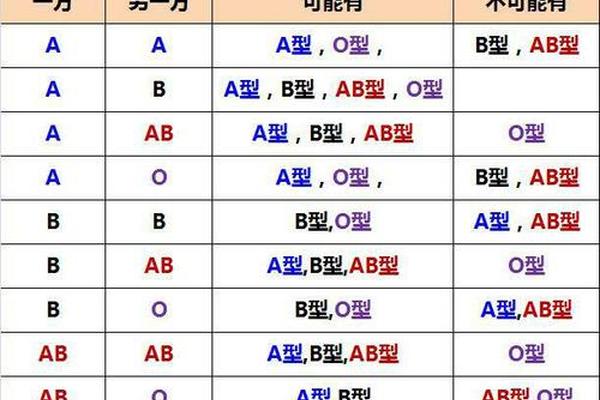
从遗传学角度,A型Rh阴性血的形成遵循ABO与Rh系统的双重遗传规律。ABO血型由9号染色体上的基因控制,父母通过显隐性基因组合决定子代血型;Rh血型则由1号染色体上的RHD和RHCE基因调控。当个体同时遗传到A型显性基因和两条隐性Rh阴性基因(如dd)时,才会表现为A型Rh阴性血。值得注意的是,由于Rh阴性基因的隐性特性,即使父母中仅有一方携带Rh阴性基因,子代仍有概率继承该特性,这使得Rh阴性血型在家族中存在隐性传播的可能。
稀有性与分布特征:地理与种族差异
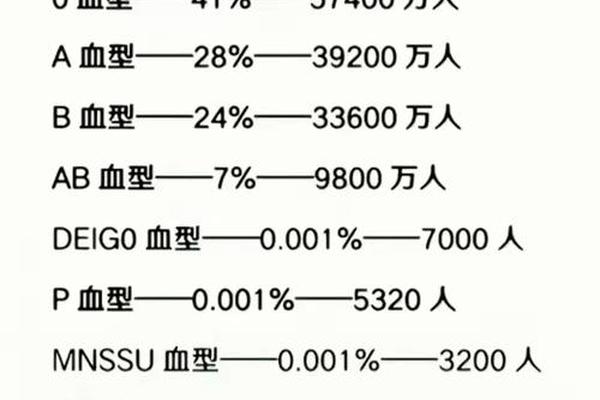
A型Rh阴性血被称为"双重稀有血型",其罕见性源于ABO与Rh系统的概率叠加。在中国汉族人群中,Rh阴性个体的总体比例仅为0.34%,其中A型Rh阴性血占比约0.102%。这意味着每万名汉族人中仅有约10人属于该血型,其稀有程度堪比大熊猫。这种分布特征与人类迁徙历史密切相关——东亚人群的Rh阴性基因频率显著低于高加索人种,后者Rh阴性比例可达15%。
从进化视角观察,Rh阴性血型可能经历过自然选择的压力。研究表明,Rh阴性母亲孕育Rh阳性胎儿时,可能引发新生儿溶血症,这种生育劣势在医疗条件落后的古代形成进化阻力。但巴斯克人群的Rh阴性比例高达40%的特殊现象提示,遗传漂变和奠基者效应在血型分布中起着重要作用。这种进化矛盾为人类学研究提供了独特样本,也解释了为何A型Rh阴性血在不同种族中呈现梯度分布特征。
临床医学中的特殊挑战:输血与生育风险
在临床实践中,A型Rh阴性血患者面临双重配型困境。首先需匹配ABO同型血液,同时必须确保供血者为Rh阴性。由于血库储备量有限,紧急情况下可采用"O型Rh阴性红细胞+A型血浆"的替代方案,但这会增加免疫反应风险。浙江大学2020年的突破性研究为此提供新思路——通过构建红细胞表面三维凝胶网络,成功将Rh阳性红细胞"伪装"成通用型,这项发表于《科学进展》的技术为稀有血型输血开辟了新途径。
对于育龄女性,A型Rh阴性血带来的生育风险更需重视。当Rh阴性母亲首次妊娠Rh阳性胎儿时,胎儿的D抗原可能诱发母体产生免疫抗体。第二次妊娠时,这些抗体会通过胎盘攻击胎儿红细胞,导致流产或新生儿溶血症。现代医学通过RhD免疫球蛋白注射可有效阻断致敏过程,使新生儿溶血症发生率从20%降至0.1%。这要求医疗机构建立完善的孕前血型筛查体系,并对Rh阴性孕妇实施全程抗体监测。
社会支持与未来展望:构建生命保障网络
面对A型Rh阴性血的特殊需求,我国已逐步建立三级保障体系。基础层面,各地血液中心通过"稀有血型之家"等组织,将献血者纳入动态数据库,北京更组建了千人级的应急献血队伍。技术层面,除浙江大学的人工红细胞改造技术外,基因编辑技术正在尝试从根本上解决血型限制,2023年《自然》期刊报道的CRISPR基因敲除技术已实现Rh阳性红细胞向阴性转化。
从公共卫生角度,需要加强三方面建设:其一,建立全国联动的稀有血型信息共享平台;其二,完善自体血储存制度,鼓励符合条件者进行术前储血;其三,推进血型转换技术的临床转化。日本学者提出的"人工造血干细胞库"概念,通过冻存稀有血型个体的干细胞实现按需造血的设想,或将成为未来发展方向。
A型Rh阴性血作为血型系统中的"双重少数",既承载着人类遗传多样性的生物学密码,也映射出现代医学应对特殊医疗需求的智慧之光。从输血安全到生育保障,从个体自救到社会共济,这个特殊血型群体面临的挑战推动着血液医学的持续进步。随着生物技术的突破性发展,人类正在突破自然血型的生理限制,这不仅是医学技术的胜利,更是对生命尊严的终极守护。未来研究应着重于血型转换技术的安全性验证、基因编辑的规范,以及全球化血液资源共享机制的建立,让每个稀有血型个体都能获得平等的生命保障。