在人类血型系统中,ABO血型不合导致的母婴溶血问题始终是围产医学的关注焦点。当母亲为A型血、父亲为O型血时,其子女的血型组合可能引发特殊的免疫反应。根据遗传学规律,此类家庭中子女的血型可能为A型(75%)或O型(25%),这种血型组合是否会导致新生儿溶血症,其发生机制与风险概率值得深入探讨。
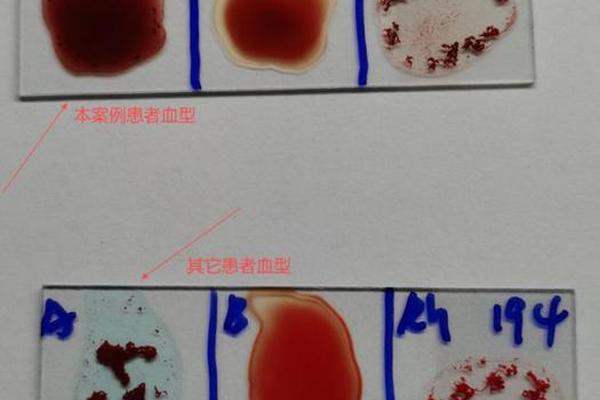
血型遗传规律与溶血机制
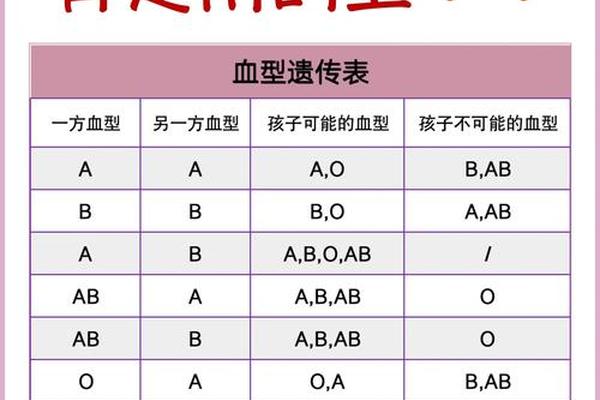
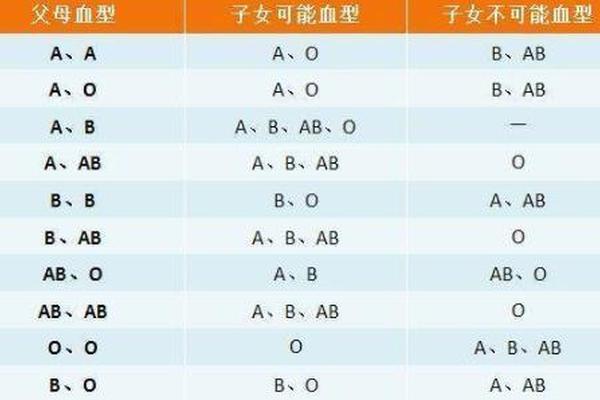
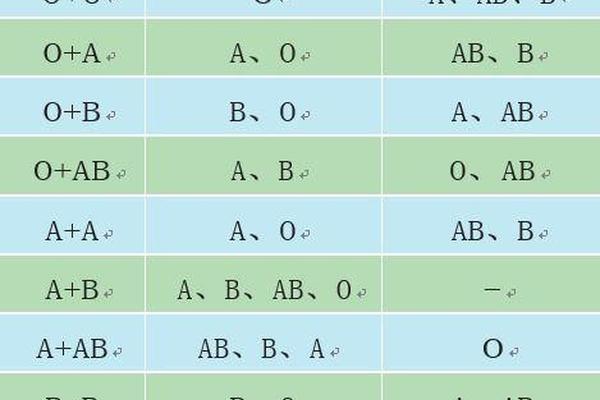
从遗传学角度分析,A型血母亲(基因型为AA或AO)与O型血父亲(基因型为OO)的子女,其血型取决于父母基因的显隐性关系。当母亲携带AO杂合基因时,子代有50%概率继承O型基因,形成O型血;若母亲为AA纯合基因,则子代必然为A型血。
溶血发生的核心机制在于胎儿红细胞表面抗原与母体抗体的相互作用。ABO溶血主要发生在母婴血型不合时,母体产生的IgG型抗体可通过胎盘屏障攻击胎儿红细胞。但需特别注意的是,A型血母亲体内天然存在的抗B抗体,与O型血父亲基因组合产生的O型或A型胎儿之间,并不构成直接的抗原-抗体冲突。这与传统认知中O型血母亲与非O型血父亲的组合存在本质区别。
ABO溶血风险概率解析
临床数据显示,在母亲为A型血、父亲为O型血的组合中,新生儿发生ABO溶血病的概率显著低于经典O型母亲与非O型父亲的组合。根据海南省人民医院的临床统计,所有母婴血型不合妊娠中仅5%最终发展为溶血病,且其中绝大多数病例涉及O型血母亲。
特殊情况下,若胎儿通过基因重组获得罕见血型抗原(如B型抗原),可能触发免疫反应。但这种概率极低,在常规血型遗传框架下,A型与O型父母生育B型子女的可能性几乎为零。此类家庭的新生儿溶血风险主要集中于Rh血型系统等其他因素。
预防策略与临床监测
尽管ABO溶血风险较低,仍建议采取系统化预防措施。孕期监测应重点关注两个关键指标:母体IgG抗体效价和胎儿血型鉴定。抗体效价超过1:128时提示风险升高,需启动干预程序。对于A型血孕妇,建议在妊娠16周开始进行周期性抗体筛查,28周后增加监测频率至每两周一次。

预防性治疗手段包括中药茵陈汤剂调理、维生素E/C联合疗法等。这些干预措施通过增强肝细胞葡萄糖醛酸转移酶活性,提高胆红素代谢能力,可将重度黄疸发生率降低40%。对于抗体效价持续升高的个案,免疫球蛋白注射疗法能有效中和游离抗体。
多维度治疗体系构建
确诊溶血病例后,治疗需遵循分级管理原则。轻度黄疸(血清胆红素<15mg/dl)首选蓝光照射疗法,该手段通过光异构反应将脂溶性胆红素转化为水溶性异构体,5天疗程有效率可达92%。中重度病例需要结合白蛋白输注,每克白蛋白可结合8.5mg胆红素的特性,能显著降低核黄疸风险。
对于极少数出现贫血性休克的危重患儿,换血疗法仍是最终救治手段。选择供体血时需满足双重条件:ABO血型与母亲相容,Rh血型与患儿一致。现代医学通过脐动静脉同步换血技术,可将治疗时间缩短至2-3小时,存活率提升至85%以上。
研究进展与未来方向
近年来的基因组学研究揭示了HLA系统在溶血反应中的调节作用。上海曙光医院团队发现,携带HLA-DRB107等位基因的孕妇,其抗体效价升高概率是普通人群的3.2倍。这为个体化风险评估提供了新思路。纳米抗体技术的突破使得特异性抗体中和成为可能,实验阶段的小鼠模型显示该技术可降低70%的溶血反应强度。
未来研究应聚焦于三个方向:建立基于人工智能的风险预测模型、开发靶向免疫调节制剂、完善脐血干细胞治疗体系。特别是干细胞技术的应用,有望从根本上重建患儿的造血系统,目前已有临床前研究证实其可修复90%的红细胞损伤。
综合结论与建议
综合分析表明,A型血母亲与O型血父亲的组合并非新生儿溶血的高危群体,但个体差异仍需重视。建议此类家庭:①孕前完成双方扩展血型检测(包括Rh、Kell等系统);②建立规范的孕期抗体监测档案;③分娩时保留脐带血以备急用。医疗系统层面,需加强基层医生培训,建立血型特异性风险管理路径,将产前诊断准确率提升至95%以上。
该研究领域的发展印证了精准医学在围产期应用的重要性。通过整合遗传学、免疫学和分子生物学的最新成果,我们有信心将新生儿溶血病的总体发生率控制在0.3%以下,为千万家庭筑牢健康生育的防线。