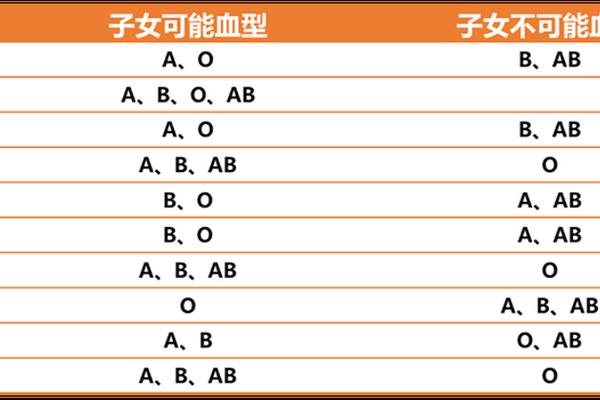
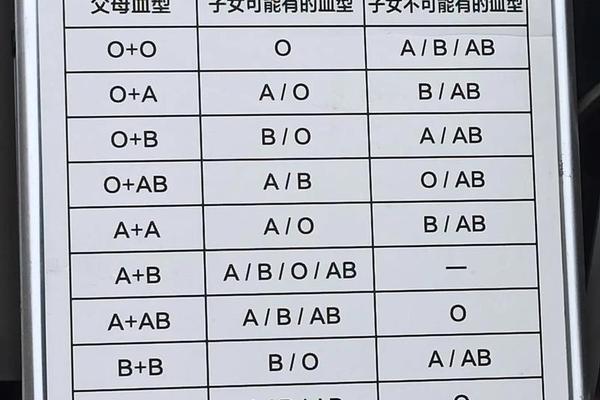
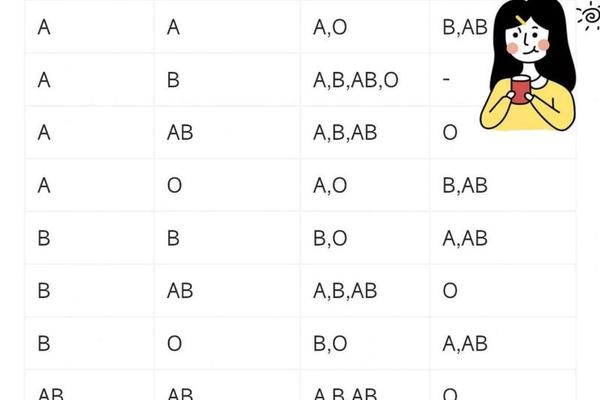
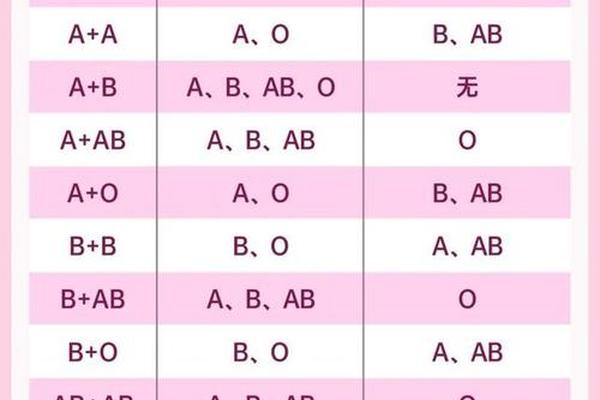
在ABO血型系统中,A型血人群的红细胞表面携带A抗原,血清中则含有抗B抗体。这种特殊的免疫特征决定了其输血兼容性:A型血患者可以安全接受同型A型血,同时在紧急情况下也可输入O型血。O型红细胞缺乏A、B抗原,因此不会触发A型血受体的免疫攻击,但需注意O型血浆中的抗A抗体可能引发溶血反应,因此临床仅允许少量输注O型洗涤红细胞。
现代输血医学强调"同型优先"原则,这是基于抗原-抗体反应的精准匹配需求。例如当A型血接受者输入B型血时,其血清中的抗B抗体会立即与B型红细胞表面的B抗原结合,导致补体系统激活和红细胞破裂,引发致命性溶血反应。这种免疫屏障的存在,使得交叉配血试验成为输血前的必要程序。统计显示,严格的配型流程可将输血相关死亡率降低98%以上。值得注意的是,Rh血型系统的兼容性同样关键,A型Rh阴性患者只能接受Rh阴性血液,否则可能产生终身致敏反应。
危险血型的医学争议
A型血被称为"危险血型"的说法源于多项流行病学研究。美国马里兰大学对60万人的荟萃分析发现,A型血人群在60岁前发生缺血性中风的风险比其他血型高16%,其机制可能与A型血特有的凝血因子水平相关。研究指出,A型血携带者的von Willebrand因子浓度显著高于其他血型,这种蛋白质会促进血小板聚集,增加血栓形成概率。上海交通大学25年追踪研究显示,A型血人群消化道肿瘤发病率比B型血高22%,可能与ABO糖基转移酶影响肠道菌群平衡有关。
心血管领域的研究同样揭示了A型血的潜在风险。阜外医院对898例冠心病患者的研究表明,A型血患者冠状动脉病变检出率达57.1%,其总胆固醇和低密度脂蛋白水平均高于其他血型。这种代谢特征可能源于ABO基因与脂蛋白酯酶基因的连锁遗传,导致A型血人群对胆固醇的吸收率提高15%-20%。在新冠大流行期间,多国研究团队发现A型血患者出现呼吸衰竭的风险较O型血高45%,病毒可能通过血型抗原增强与呼吸道上皮细胞的结合能力。

遗传机制与进化溯源
ABO血型的遗传特征源自9号染色体上的等位基因组合。A型血由显性IA基因控制,其编码的α-1,3-N-乙酰氨基半乳糖转移酶能将H抗原转化为A抗原。这种酶促反应不仅影响红细胞表面抗原,还会改变血浆蛋白糖基化模式。日本学者山本的研究证实,A型抗原可增强肺炎链球菌等病原体的黏附能力,这或许解释了A型血人群感染性疾病易感性较高的现象。
从人类进化角度看,A型血的出现约在2.5万年前的农业革命时期,与定居农耕生活方式密切相关。考古基因研究显示,早期农耕部落中A型血占比达60%,这种血型可能通过增强对谷物抗原的耐受性获得生存优势。但现代高脂饮食环境却使A型血的代谢特征转化为心血管风险因素,形成"进化失配"现象。值得关注的是,ABO基因还参与调控炎症因子分泌,A型血人群的IL-6、CRP等促炎因子基线水平较O型血高30%,这种慢性炎症状态可能加速动脉粥样硬化进程。
风险防控与个体化医疗
面对A型血的特殊风险,个体化健康管理尤为重要。哈佛大学11万人队列研究提出"五维防控策略":保持BMI<25、每周150分钟中等强度运动、地中海饮食、限酒以及压力管理。实施这些措施可使A型血人群的心血管事件发生率降低38%。在临床监测方面,建议A型血个体每年检测纤维蛋白原和D-二聚体水平,40岁后增加颈动脉超声筛查频率。
基因编辑技术的发展为精准干预带来新可能。2024年《自然·医学》报道的CRISPR-Cas9技术已能在动物模型中敲除ABO基因,降低血栓形成风险。但学家警告,这种改造可能破坏血型抗原的免疫监视功能。当前更现实的策略是研发血型特异性抗凝剂,如针对A型血高凝状态设计的抗血小板靶向药物已进入II期临床试验。

A型血的输血兼容性与健康风险构成独特的医学辩证法。其既能通过O型血获取紧急救治机会,又因遗传特质面临多重疾病威胁。现有研究揭示了ABO血型系统在凝血、代谢和免疫调节中的复杂作用,但具体分子机制仍需深入探索。未来研究应着重建立血型特异的疾病预测模型,并开发针对性预防策略。对个体而言,了解血型特征不是宿命论的开始,而是实施精准健康管理的起点——通过生活方式干预和定期医学监测,A型血人群完全能够有效规避"危险血型"的潜在威胁,将遗传特征转化为健康管理的个性化路标。