在医学与生命科学的探索中,人类对血型的认知早已超越了简单的ABO分类。当人们谈论“熊猫血”时,往往联想到的是一种神秘而珍贵的血液——Rh阴性血型。这种仅占汉族人口0.3%-0.4%的稀有血型,因其稀缺性被冠以“熊猫血”之称。但鲜为人知的是,在血型抗原的复杂谱系中,其背后隐藏着精妙的遗传规律、临床医学的重大挑战以及关乎生命存续的社会命题。本文将从科学本质、遗传特性、临床影响及社会支持四个维度,深度解析这一特殊血型的奥秘。
血型系统的双重密码
人类红细胞表面覆盖着超过300种抗原,构成35个已被国际认可的血型系统。其中ABO系统决定血液的“基础身份”,而Rh系统则通过D抗原的存在与否划分出Rh阳性(Rh+)与Rh阴性(Rh-)两大阵营。当红细胞缺乏D抗原时,便成为Rh阴性个体,即俗称的“熊猫血”。
这种分类的科学依据源自抗原-抗体反应机制。Rh阴性个体的血浆中原本不含抗D抗体,但若输入Rh阳性血液,免疫系统将识别D抗原为“入侵者”并产生抗体。首次接触尚可耐受,但二次输入则可能引发致命性溶血反应,导致红细胞破裂、血红蛋白外流,进而引发休克或急性肾衰竭。这种免疫特性使得Rh阴性血液的输注必须遵循严格的血型匹配原则。
遗传图谱中的隐形基因
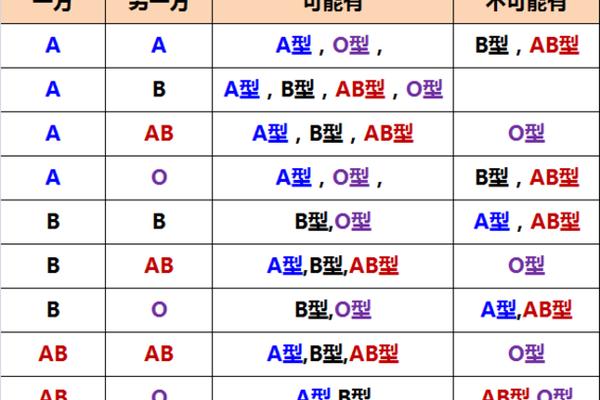
Rh血型的遗传遵循孟德尔定律,由位于1号染色体上的RHD基因控制。显性基因D决定Rh阳性,隐性基因d则对应Rh阴性。若父母双方均为Rh阴性(dd),子女必然遗传隐性基因;若一方为显性杂合(Dd),则有50%概率传递隐性基因;而显性纯合(DD)父母则无法生育Rh阴性后代。
这种遗传特性在临床孕育中产生深远影响。当Rh阴性母亲怀有Rh阳性胎儿时,胎儿红细胞可能通过胎盘渗入母体,触发抗D抗体生成。首胎尚可通过胎盘屏障保护,但第二胎时抗体将穿越胎盘攻击胎儿红细胞,导致新生儿溶血病,严重时可致胎儿水肿或死亡。Rh阴性孕妇需在孕28周及产后72小时内注射抗D免疫球蛋白,以中和抗原、阻断免疫应答。
临床救治的双刃剑
在紧急输血场景中,Rh阴性血型的稀缺性可能成为生死攸关的瓶颈。我国建立的“冰冻红细胞”技术可将Rh阴性血液在-65℃下保存十年,但突发性大出血仍需依赖即时血源供应。值得关注的是,约25%初筛Rh阴性个体实为“亚洲型Del”变异型,其红细胞表面仍存在微量D抗原,可安全接受Rh阳性血液。通过分子检测技术鉴别真伪阴性,可有效缓解血源压力。
对于恶性肿瘤患者,血型特性更与治疗方案深度交织。研究发现,急性髓系白血病细胞表面CD86分子的异常表达可能影响T细胞免疫功能,而Rh阴性淋巴瘤患者对特定化疗药物的敏感性差异,提示血型抗原可能参与肿瘤微环境调控。这些发现为个体化治疗开辟了新视角。
生命之网的共同编织
建立稀有血型数据库已成为全球共识。我国推行的“自体储血”方案,建议Rh阴性个体在妊娠晚期储存200-400ml自体血,同时“中国稀有血型库”通过志愿登记实现精准匹配。北京、广州等地开展的“熊猫侠”互助行动,已形成覆盖全国的应急网络,2021年仅稀有血型永和救援团队即动员430名志愿者定向献血。

专家呼吁推行全民血型普查,在医保卡、身份证中嵌入血型信息。浙江大学附属医院开展的Rh阴性献血者宣教计划,通过基因检测技术发展出稳定的献血者队伍,使临床用血保障率提升至92%。这些实践表明,科技赋能与社会动员的结合,是破解稀有血型困境的关键路径。
从遗传密码到临床救治,从个体命运到群体共济,“熊猫血”的特殊性既彰显着生命科学的精妙,也暴露出医疗体系的脆弱环节。当前亟需建立国家层面的稀有血型动态监测网络,推进Del型精准鉴别技术的临床应用,同时加强公众科普教育。未来,随着基因编辑技术的发展,或可通过体外诱导多能干细胞分化为Rh阴性红细胞,从根本上突破血源限制。每一份稀有血液的守护,都是对人类生命共同体的庄严承诺。