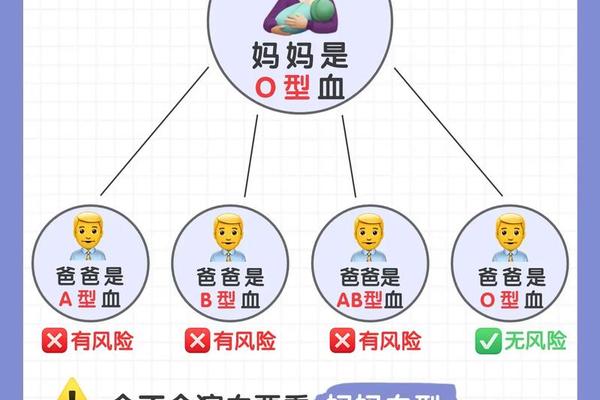
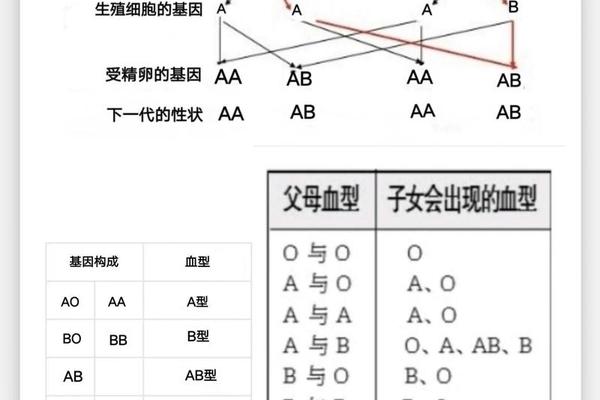
人类ABO血型系统是红细胞表面抗原差异的集中体现,其中A型血的特征在于红细胞携带A抗原。从分子层面看,A抗原的合成由9号染色体上的A等位基因(IA)调控,该基因编码的α-1,3-N-乙酰半乳糖胺转移酶,能将H抗原末端的半乳糖转化为A抗原。值得注意的是,A基因对O基因呈显性遗传,因此基因型为AA或AO的个体均表现为A型血,而仅当双隐性基因O(ii)纯合时才会形成O型血。
A型血内部存在复杂的亚型分化,如A1与A2亚型占比超过99%。A1亚型的红细胞表面同时存在A和A1抗原,而A2亚型仅含A抗原。这种差异源于基因突变导致的酶活性变化:A1转移酶可催化3型H链生成A抗原,而A2转移酶则缺乏此功能,导致A2型红细胞的A抗原数量显著减少,且H抗原表达量更高。血清学检测中,约1%-2%的A2型个体血清中会存在抗-A1抗体,可能引发输血反应,这要求临床血型鉴定需结合正反定型法以降低误判风险。

二、A型血与其他血型的生物学比较
在ABO系统中,A型血与B型血的抗原差异源于转移酶底物特异性:B型基因编码的α-1,3-半乳糖转移酶将H抗原转化为B抗原。AB型则是同时表达两种抗原的嵌合状态。从群体分布看,中国汉族中A型占比约27%,略低于O型的41%,但显著高于B型的26%和AB型的6%。这种分布差异可能与不同血型对传染病的免疫适应性有关,例如研究发现A型血人群更易感染诺如病毒,而O型血对疟疾的抵抗能力更强。
在输血相容性方面,A型血清含抗-B抗体,可攻击B或AB型红细胞。因此A型个体仅能接受A型或O型血液。值得注意的是,O型血浆中的抗-A抗体虽在少量输血时可通过受血者血清稀释,但大量输注仍可能引发溶血反应,这颠覆了传统“万能供血者”的认知。对于Rh血型系统,我国A型人群中Rh阴性仅占0.3%-0.5%,这类个体若接受Rh阳性血液,可能通过免疫作用产生抗-D抗体,影响妊娠或二次输血安全。
三、A型血的临床关联与健康启示
流行病学研究揭示了A型血与特定疾病的关联性。一项纳入510万人的瑞典队列研究发现,A型血人群的静脉血栓形成风险较O型血高20%,这可能与A型个体凝血因子VIII水平较高相关。我国阜外医院研究进一步证实,A型血人群的低密度脂蛋白胆固醇水平显著升高,冠心病患病风险增加15%。在肿瘤领域,A型血与胃癌、结直肠癌的关联性已获多项研究支持,机制可能涉及幽门螺杆菌感染率差异及ABO糖基转移酶对肿瘤微环境的调控。
在器官移植领域,供受体ABO血型匹配是移植成功的基石。近年研究发现,A型供体的肾脏移植给O型受体时,通过血浆置换清除抗-A抗体可实现跨血型移植,这为缓解器官短缺提供了新思路。基于血型抗原开发的肿瘤疫苗已进入临床试验阶段,例如针对A型糖链设计的乳腺癌疫苗,在动物模型中显示出特异性免疫激活效果。
四、技术发展与未来研究方向
现代分子诊断技术极大提升了血型检测精度。PCR-SSP法可区分A1/A2亚型,质谱技术能定量分析红细胞膜抗原密度,而单细胞测序技术甚至可追溯造血干细胞分化过程中的抗原表达动态。在法医学领域,血型检测已从传统的血清学方法转向STR基因分型,但ABO基因座的多态性分析仍为个体识别提供辅助信息,例如ABO基因启动子区rs8176746位点的C/T多态性可追溯父系遗传特征。
未来研究需重点关注三个方向:一是建立中国人群A亚型数据库,完善稀有血型冷冻保存体系;二是深入解析ABO糖基转移酶非编码区变异对酶活性的调控机制;三是开发基于血型分子特征的个性化医疗方案,例如针对A型血人群的心血管疾病预防策略。随着基因编辑技术的成熟,定向修饰造血干细胞的ABO基因或将成为实现通用型血液制品的突破点。
通过对A血型的系统剖析可见,这一看似简单的生物学标记实则蕴含复杂的遗传密码与临床价值。从抗原合成的分子机制到疾病易感性的群体特征,A型血的科学研究不断刷新人类对生命本质的认知。随着精准医学时代的到来,血型研究将突破传统输血匹配的范畴,在疾病预警、治疗靶点发现等领域发挥更深远的作用。建议医疗机构加强血型数据的多组学整合,同时开展公众科普消除“血型决定论”误区,让这一百年发现真正服务于人类健康。