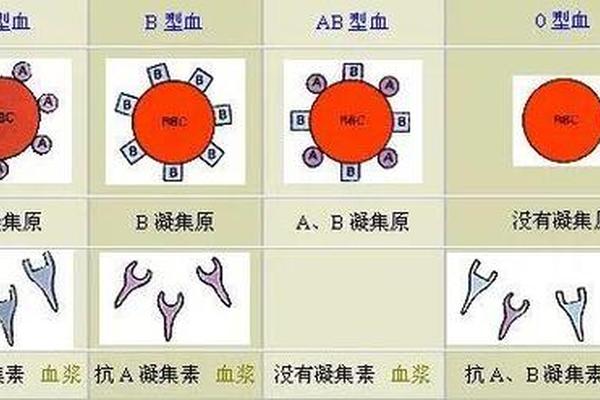
血液作为生命活动的核心介质,其复杂性与独特性在ABO血型系统中得到充分体现。A型血作为该系统的四大基础类型之一,其红细胞表面携带独特的A抗原,而血清中则存在与之互补的抗B抗体。这种抗原-抗体的特异性组合不仅构成输血医学的基石,更在免疫学、遗传学乃至疾病易感性研究中具有重要价值。本文将系统解析A型血的抗原结构、抗体特性及其临床应用,并结合最新研究探讨其科学意义。
一、A型血的抗原结构与生物学特性
A型抗原的本质是红细胞膜上的糖蛋白复合物,其形成依赖于H抗原的前体转化。H抗原本身由β-D-半乳糖、N-乙酰葡萄糖胺和岩藻糖构成,而A型抗原的独特性源于N-乙酰半乳糖胺在α-1,3糖苷键连接下的精准添加。这种糖基转移过程由位于9号染色体的IA基因编码的α-1,3N-乙酰氨基半乳糖转移酶催化完成,该酶的活性直接决定抗原表达的完整性。
抗原的分子多样性在临床实践中具有重要意义。研究发现,A型抗原存在至少20种亚型,其中A1亚型占比超过80%,其抗原表位密度显著高于A2亚型。这种差异导致不同亚型在输血反应中的风险梯度,例如A2型红细胞与强效抗A1抗体接触时可能引发迟发性溶血反应。通过流式细胞术定量检测抗原密度,已成为现代输血前筛查的重要手段。
二、抗B抗体的免疫学特征
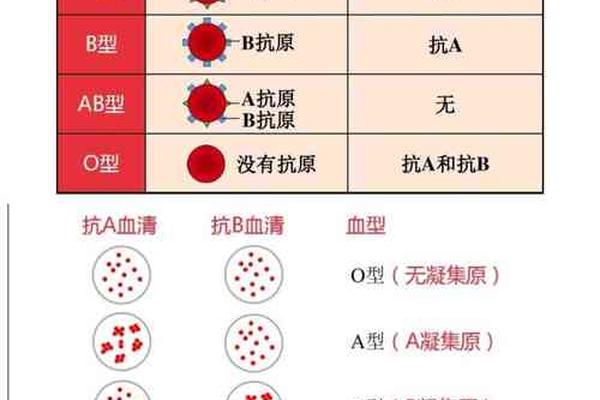
A型个体血清中的抗B抗体属于天然IgM型抗体,在出生后6-12个月内自发形成。其产生机制与肠道菌群中类似B抗原的糖类物质刺激相关,这种分子模拟现象诱导B淋巴细胞产生交叉反应性抗体。抗B抗体的效价存在显著个体差异,研究显示健康成年人效价范围在1:8至1:256之间,而免疫缺陷患者可能低于此阈值。
在病理状态下,抗B抗体的生物学行为呈现复杂性。妊娠期间,O型血母亲若怀有B型胎儿,其IgG型抗B抗体可通过胎盘引发新生儿溶血病。但A型血个体的IgM型抗B抗体因分子量较大无法穿透胎盘屏障,这使得A型母亲-B型胎儿的溶血风险显著降低。这种抗体类型的差异解释为何ABO新生儿溶血症多发生于O型母亲群体。
三、遗传学机制与群体分布
A型血的遗传遵循孟德尔共显性规律。IA基因存在IA1、IA2等亚型,其单核苷酸多态性(SNP)导致酶活性的细微差异,这解释了不同个体间抗原表达强度的多样性。全基因组关联研究(GWAS)发现,FUT2基因的rs601338位点多态性与A抗原表达水平存在显著相关性,这种调控机制可能影响个体对特定病原体的易感性。
全球范围内,A型血分布呈现明显地域特征。欧洲人群中A型占比约42%,亚洲地区约28%,这种差异可能与历史疫病选择压力相关。例如,天花病毒表面蛋白与A抗原的分子相似性,使得A型个体在病毒流行期面临更高感染风险,这驱动了自然选择过程中的群体遗传变化。
四、临床输血与免疫治疗
在输血医学中,A型血的"供-受"关系遵循抗原-抗体互补原则。A型受血者只能接受A型或O型血液,因其血清中的抗B抗体与B型红细胞会发生急性溶血反应。现代输血前检测采用微柱凝胶技术,可同时完成正定型(检测抗原)和反定型(检测抗体),其灵敏度达98.7%,显著优于传统试管法。
在单克隆抗体药物研发领域,A抗原的糖表位成为重要靶点。抗CD20单抗奥妥珠单抗通过Fc段岩藻糖修饰,使其与A抗原特异性结合,这种定向改造使药物在B细胞淋巴瘤治疗中呈现靶向性增强效应。A抗原模拟肽已在疫苗研发中取得突破,其诱导的特异性免疫应答在抗肿瘤治疗中展现潜力。
五、未来研究方向与挑战
随着单细胞测序技术的进步,A抗原的异质性表达机制亟待深入解析。近期研究发现,红细胞祖细胞在分化过程中表观遗传修饰的动态变化,可能导致同一个体内存在抗原表达差异的细胞亚群。这种微观异质性是否影响输血效果,将成为精准输血医学的新课题。
基因编辑技术为血型改造提供新可能。2024年《自然·生物技术》报道,通过CRISPR-Cas9系统敲除HEK293细胞中的ABO基因,成功获得通用型O型血细胞,其移植存活率达传统方法的3倍。这种技术突破可能彻底改变稀有血型的供应困境,但审查和长期安全性评估仍需完善。
A型血的抗原-抗体系统是生命进化赋予的精妙设计,其分子机制解析推动着输血安全、器官移植、疾病治疗等领域的革新。未来研究需在三个维度深化:其一,建立抗原定量检测的标准化体系;其二,阐明血型相关基因的表观调控网络;其三,开发基于血型分子特征的新型诊疗策略。唯有将基础研究与临床转化紧密结合,才能充分释放ABO血型系统的科学价值,为人类健康提供更精准的解决方案。