ABO血型系统中A抗原低表达的临床与分子机制研究
ABO血型系统自1900年被发现以来,始终是输血医学和临床诊断的核心议题。在这一系统中,A抗原的表达水平差异可显著影响血型判定的准确性与临床治疗的安全性。部分个体的红细胞表面A抗原呈现低表达状态,导致正反定型不符或血型误判,甚至可能引发输血反应或器官移植排斥。近年来,随着分子生物学技术的发展,A抗原低表达的机制逐渐被揭示,但其临床意义与遗传学背景仍需系统性探讨。本文将从抗原低下的成因、临床影响、检测方法及未来研究方向等方面展开分析。
一、抗原低表达的成因
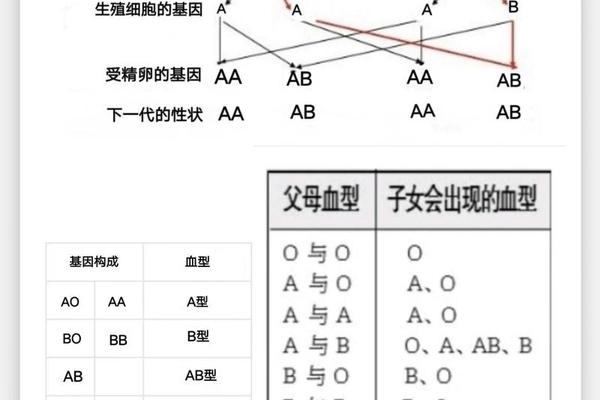
A抗原低表达的分子机制主要与ABO基因的遗传变异相关。ABO基因位于9号染色体(9q34.1-q34.2),其编码的糖基转移酶负责将N-乙酰半乳糖胺(A抗原)或半乳糖(B抗原)添加到H抗原前体上。研究发现,某些基因突变可导致酶活性降低或结构异常,进而影响抗原表达。例如,启动子区域-119位C>T突变或第7外显子1054位点碱基缺失,可能通过干扰转录效率或酶功能引发A抗原表达减弱。ABO亚型(如A2、A3等)的基因型差异也会导致抗原强度的显著变化,例如A2型个体的A抗原密度通常低于A1型。
除遗传因素外,疾病状态也可能导致抗原表达异常。例如,白血病、恶性肿瘤等疾病患者的免疫功能受损或红细胞生成异常,可能通过抑制糖基转移酶的活性或改变红细胞膜结构,使A抗原呈现暂时性减弱。研究显示,白血病患者中约40%出现ABO抗原减弱现象,其中A型抗原的减弱比例显著高于其他血型。此类抗原低表达现象在疾病缓解后可能恢复,提示其动态变化的复杂性。
二、临床意义与挑战
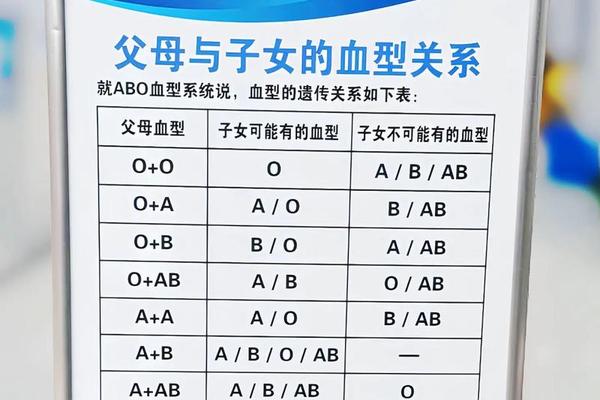
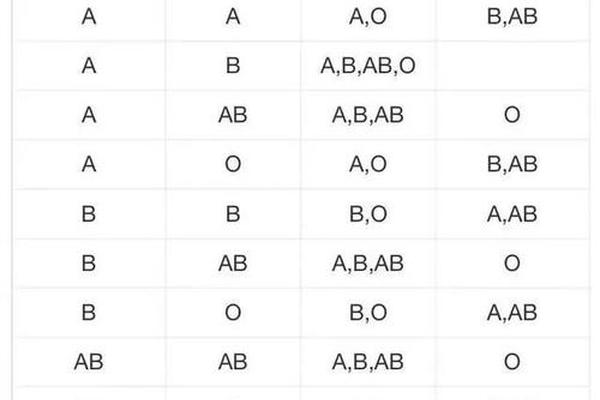
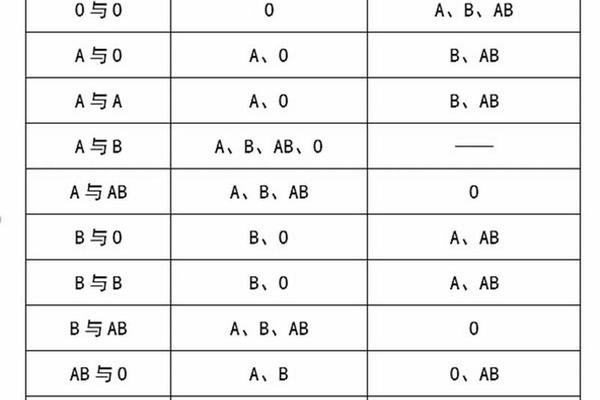
A抗原低表达对输血安全构成直接威胁。根据输血原则,供者红细胞抗原与受者血清抗体的相容性是关键。若A抗原低表达患者的血液被误判为O型,输入含有抗A抗体的血浆时,可能引发急性溶血反应。研究显示,ABO血型不合输血的致死率高达90%以上,其中抗原表达异常是重要诱因之一。例如,一例白血病患者的A抗原因治疗暂时减弱,首次输血被误判为O型,导致后续输血时发生严重溶血。临床需通过多方法验证血型,避免此类风险。
A抗原低表达与疾病关联性研究逐渐受到关注。妊娠并发症研究中发现,O型女性因缺乏A/B抗原,其血管内皮细胞H抗原暴露可能增加子痫前期风险,而A抗原低表达个体的相关风险尚未明确。肿瘤学领域亦有研究提示,A抗原表达异常可能影响肿瘤细胞的免疫逃逸机制,但其具体机制仍需进一步探索。这些发现提示,抗原低表达不仅是血型判定的技术问题,更可能成为疾病诊疗的生物标志物。
三、检测技术与策略优化
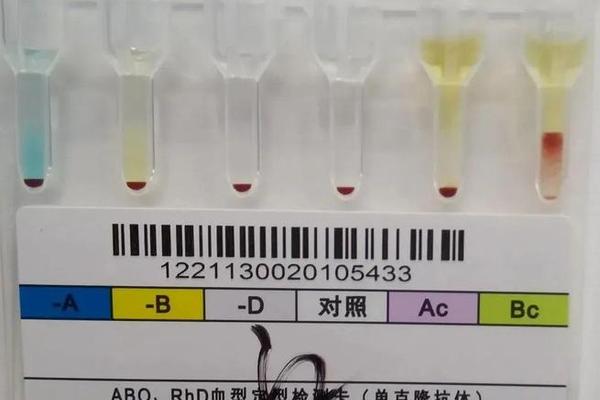
针对A抗原低表达的检测,需结合血清学与分子生物学方法。传统的微柱凝胶法和盐水试管法通过凝集反应强度判断抗原水平,但灵敏度有限。例如,某研究采用单克隆抗体检测发现,抗原减弱组的凝集效价仅为正常组的1/8,需通过吸收放散试验进一步验证。近年来,基因测序技术被应用于ABO亚型鉴定,例如对启动子区域和外显子的深度测序可识别-35_-18位碱基缺失等罕见突变。这种多技术联用策略显著提高了低表达抗原的检出率。
临床实践中,对于疑似抗原低表达病例,建议采用分步检测流程:首先通过增强凝集试验(如抗人球蛋白试验)确认抗原存在,再通过唾液血型物质检测或基因测序明确分子机制。例如,一例A抗原减弱患者经唾液检测确认分泌型特征,结合基因测序发现新型启动子突变,最终避免了输血误判。此类案例凸显了综合检测的重要性。
四、未来研究方向
未来研究需聚焦于A抗原低表达的分子机制与临床应用。建立大规模人群基因数据库,系统分析ABO基因变异与抗原表达的关系,尤其是罕见突变的功能验证。探索抗原低表达在疾病发生中的作用,例如其是否影响肿瘤微环境或妊娠期血管重塑。开发快速、低成本的基因分型技术,将有助于基层医疗机构实现精准血型鉴定。
在临床管理层面,建议制定抗原低表达患者的输血规范,例如优先选择同型输血或经辐照处理的血液制品。加强多学科协作(如血液科、遗传学与产科),推动个体化诊疗方案的制定。例如,对妊娠合并A抗原低表达的孕妇,需动态监测抗体效价,预防胎儿溶血风险。
A抗原低表达是ABO血型系统中的复杂现象,其成因涉及遗传变异、疾病状态及环境因素。临床中,抗原低表达可能导致输血风险、疾病误诊及治疗困难,需通过多技术联用实现精准检测。未来研究应深入解析其分子机制,并探索其在疾病诊疗中的潜在价值。通过整合基因组学、临床医学与输血技术,有望为抗原低表达患者提供更安全的医疗干预策略,推动精准医学的发展。